|
Гипермаркет знаний>>Химия>>Химия 10 класс>> Химия: Теория строения органических соединений A. M. Бутлерова
Органическая химия как наука оформилась в начале XIX в., когда шведский ученый Й. Я. Берцелиус впервые ввел понятие об органических веществах и об органической химии. Первая теория в органической химии — теория радикалов. Химиками было обнаружено, что при химических превращениях группы из нескольких атомов в неизменном виде переходят из молекулы одного вещества в молекулу другого вещества, подобно тому как переходят из молекулы в молекулу атомы элементов. Такие «неизменяемые» группы атомов и получили название радикалов.
Однако далеко не все ученые были согласны с теорией радикалов. Многие вообще отвергали идею атомистики — представления о сложном строении молекулы и существовании атома как ее составной части. То, что неоспоримо доказано в наши дни и не вызывает ни малейших сомнений, в XIX в. было предметом ожесточенных споров.
Теорию радикалов сменила теория типов, в соответствии с которой предполагалось, что реакции органических веществ сходны с реакциями простейших неорганических соединений. Основоположник этой теории Ш. Жерар предложил разделить органические вещества на группы, близкие по своему типу к воде, хлористому водороду, аммиаку и т. д.
Потерпело поражение и учение о «витализме», которое не устояло перед достижениями практической химии.
Органическая химия накапливала все больше фактов о соединениях углерода, количество которых возрастало. Объяснить причины такого многообразия органических веществ ученые не могли. Еще больше вопросов вызывало существование изомеров. Эти вещества имели совершенно одинаковый состав, но проявляли при этом разные и физические, и химические свойства. Ужб известный вам Фридрих Вёлер в одном из писем Берцелиусу так описывал органическую химию того времени: «Органическая химия может сейчас кого угодно свести с ума. Она кажется мне дремучим лесом, полным удивительных вещей, безграничной чащей, из которой нельзя выбраться, куда не осмеливаешься проникнуть...» Большое влияние на развитие химии в это время оказали работы английского химика К. Э. Франкланда, который, опираясь на идеи атомистики, в 1853 г. ввел понятие «валентность». Однако валентность углерода во многих соединениях, таких, например, как этан С2Н6 и пропан С3Н8, вызывала еще больше вопросов. В 1857 г. немецкий химик Ф. А. Кекуле отнес углерод к четырехвалентным элементам, а в 1858 г. он одновременно с шотландским химиком А. Купером отметил, что атомы углерода способны соединяться друг с другом в различные цепи.
Однако за уже установленными фактами и частными выводами и Франкланд и Кекуле не увидели общей концепции.

Немецкий химик-органик. Его исследования были сосредоточены в области теоретической органической химии и органического синтеза. Высказал мысль о валентности как о целом числе единиц сродства, которым обладает атом (1857). Углерод считал четырехвалентным элементом (как и А. В. Г. Кольбе).

Русский химик, академик Петербургской АН (с 1874 г.). Создатель теории химического строения органических веществ (1861). Предсказал и изучил изомерию многих органических соединений. Синтезировал многие вещества.
Оставался открытым вопрос, как определять строение молекулы. Была необходима научная теория органических соединений. Такая теория была создана русским ученым Александром Михайловичем Бутлеровым. Именно его пытливый ум «осмелился проникнуть» в «дремучий лес» органической химии и начать преобразования этой «безграничной чащи» в залитый солнечным светом регулярный парк с системой дорожек и аллей. Основные идеи новой теории впервые были высказаны Бутлеровым в 1861 г. в докладе «О химическом строении веществ» на съезде немецких естествоиспытателей и врачей в г. Шпейере.
Кратко сформулировать положения и следствия теории строения А. М. Бутлерова можно следующим образом:
1. Атомы в молекулах веществ соединены согласно их валентности. Углерод в органических соединениях всегда четырехвалентен, а его атомы способны соединяться друг с другом, образуя различные цепи.
2. Свойства веществ определяются не только их качественным и количественным составом, но и порядком соединения атомов в молекуле, т. е. химическим строением вещества.
3. Свойства органических соединений зависят не только от состава вещества и порядка соединения атомов в его молекуле, но и от взаимного влияния атомов и групп атомов друг на друга. (Наибольшее влияние оказывают атомы, непосредственно связанные друг с другом. Влияние атомов или групп атомов, не связанных непосредственно, ослабевает по мере их удаления друг от друга.)
Рассмотрим подробнее положения теории строения органических соединений. Свойства вещества зависят от того, из каких атомов состоит его молекула. Молекула метана СН4 состоит из атомов углерода и водорода. Это вещество при обычных условиях — газ, который вступает в химические реакции с трудом. В состав молекул метилового спирта СН3ОН, помимо атомов углерода и водорода, входит атом кислорода. Метиловый спирт в тех же условиях — это уже жидкость, которая способна реагировать с различными веществами, например с серной кислотой, металлическим натрием. Различные свойства этих соединений обусловлены их различным качественным составом.
В то же время могут отличаться и свойства веществ с одинаковым качественным составом. Например, если метан СН4 начинает реагировать с хлором или бромом только при ультрафиолетовом освещении или нагревании, то этилен С2Н4, как вы знаете, присоединяет эти галогены даже в темноте и без нагревания (обесцвечивает бромную воду). Ацетилен, подобно этилену, легко реагирует с бромом в темноте, тогда как бензол вступает в реакцию с бромом только в присутствии катализатора. Ацетилен С2Н2 и бензол С6Н6 имеют одинаковый качественный состав и простейшую формулу СН (на один атом углерода в их молекулах приходится один атом водорода), но отличаются по количественному составу, что отражают их молекулярные формулы. Различие в количественном составе этих веществ вызывают их различные химические свойства.
Вещества, которые имеют одинаковый состав, а значит, и одинаковую молекулярную массу, также могут отличаться по свойствам, если они имеют различное химическое строение. Такие вещества, как вы знаете, называются изомерами, а явление — изомерией. Причиной изомерии является различный порядок расположения атомов в молекуле. Молекулярная формула показывает только качественный и количественный состав соединения, но не несет информации о порядке связей атомов в молекуле. Так, для молекул формулы С4Н10 возможны два различных порядка связи атомов углерода в цепи. К цепи из трех атомов углерода четвертый углеродный атом может быть присоединен двумя способами: либо к одному из крайних атомов, либо к среднему атому, сохраняя четырехва-лентность. Действительно, молекулярная формула С4Н10 соответствует двум различным соединениям, отличающимся расположением атомов в молекулах: нормальному бутану (н-бутану), т. е. соединению, содержащему неразветвленную цепь атомов углерода, и изобутану, молекула которого имеет разветвленное строение.
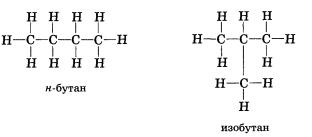
Физические свойства этих соединении отличаются: изооу-тан имеет более низкие температуры кипения и плавления, чем « бутан. Химические свойства данных изомеров различаются незначительно, так как они имеют одинаковые качественный состав и характер связи между атомами в молекуле.
Таким образом, с точки зрения теории А. М. Бутлерова существование изомеров — не загадочное явление, противоречащее представлениям людей об окружающем мире, а закономерный результат вариативности соединения атомов в молекуле.
Очевидно, что способность атомов углерода соединяться друг с другом и образовывать «цепи» легко объясняет «неправильную» формальную валентность углерода в этане С2Н6, пропане С3Н8 и других органических соединениях. Структурные формулы, например, бутана и изобутана лишь подтверждают это.
Различное количество атомов углерода в молекулах и их способность, соединяясь друг с другом, образовывать разные комбинации («скелеты» молекул) делают понятной причину многообразия органических веществ.
Подводя итоги, необходимо заметить, что теория строения органических соединений возникла не случайно, предпосылками ее создания явились:
• накопление большого количества разрозненных фактов об органических веществах и их свойствах;
• наличие неясностей и противоречий в известном фактическом материале;
• работы предшественников А. М. Бутлерова и его собственная работа.
опорный каркас урока химии 10 класса, самопроверка по химии, мультимедиа для всех классов
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|













