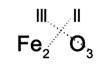|
Гіпермаркет Знань>>Хімія>>Хімія 7 клас. Повні уроки>>Хімія: Валентність хімічних елементів. Визначення валентності за формулами бінарних сполук. Повні уроки
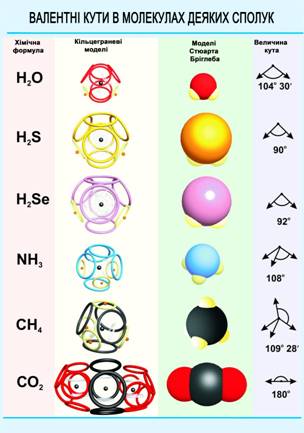
Мета уроку1. Засвоїти поняття валентність; Хід урокуВалентність хімічних елементівВалентність елемента - це його здатність утворювати певне число хімічних зв'язків. За кількістю рисок у вже знайомих нам формулах декількох молекул видно, що водень і хлор одновалентних, кисень - двовалентний, а азот - трьохвалентний. Валентність визначається як кількість електронних пар, якими даний атом пов'язаний з іншими атомами.
Оскільки в хімічному зв'язку беруть участь тільки електрони зовнішніх оболонок, такі електрони називають валентними. Одинична (проста) ковалентний зв'язок виникає, коли атоми ділять між собою одну пару валентних електронів. Структурні формули наглядно показують послідовність зв'язування атомів в молекулі і валентність елементів, проте якщо така докладна інформація не потрібна, молекули можна записувати у вигляді скорочених хімічних формул. Наприклад, вже знайомі нам молекули в цьому випадку виглядають так: Але як визначають валентності елементів? Для цього можна скористатися нашими знаннями про будову зовнішніх електронних оболонок атомів, як ми це вже робили при визначенні валентностей водню, хлору, натрію, фтору, кисню та азоту в їх конкретних хімічних сполуках.
Деякі елементи виявляють в будь-яких з'єднаннях одну і ту ж валентність. Такі, наприклад, водень, натрій, калій, срібло, фтор (валентність I); або магній, кальцій (валентність II). Інші елементи можуть - в залежності від партнерів по хімічній реакції - проявляти кілька різних валентностей. У той час, коли хіміки ще нічого не знали про будову атомів, вони успішно визначили валентності багатьох елементів за даними хімічного аналізу. Аналіз дозволяє з'ясувати склад з'єднання, тобто кількісне співвідношення атомів різних елементів у молекулі - молекулярну формулу. Робиться це шляхом точного визначення маси кожного елемента в зразку, ретельно очищеному від домішок інших речовин. З методикою аналізу ви докладно познайомитеся в 10 класі. Зараз же ми скористаємося результатами вже проведеного аналізу для визначення валентності, наприклад, азоту. Ще одне спостереження: кисень у всіх з'єднаннях двовалентний. Тому, наприклад, в поєднанні SO2 валентність сірки може бути тільки IV (валентність кисню II помножити на 2 атоми кисню = 4), а в з'єднанні SO3 валентність сірки - VI (валентність кисню II помножити на 3 атоми кисню = 6). У більш складних випадках можна дати лише часткову відповідь, але і він буває корисний. Наприклад, про з'єднання HClO4 ми можемо лише сказати, що залишок ClO4 - одновалентний (так як ми відняли від нього одновалентних атом водню). У поєднанні H2SO4 залишок SO4 - двовалентний (відняли два одновалентних атома водню). Тому для визначення валентності якого-небудь елемента годяться тільки його прості з'єднання з воднем і киснем, що містять тільки один атом досліджуваного елемента. Вимога простоти досить істотно. Наприклад, за складом з'єднання СН4 (метан) можна правильно укласти, що елемент вуглець чотиривалентним. Але існує і складне з'єднання вуглецю С6Н4 (бензол), за яким судити про валентності вуглецю тільки з результатів аналізу важко. Будь ласка, перегляне цей науковий відео матеріал
Контролюючий блок №11. Розкрийте поняття «валентність». Визначення валентності за формулами бінарних сполукАдже зараз розберемося в тому, як складають молекулярні формули за вже відомим валентності елементів. Нам потрібно навчитися робити це для складних речовин, що складаються з двох елементів.
Тепер зробимо перевірку. Два атома 3-х валентного заліза дадуть в сумі (2 х III = 6) вільних валентностей і стільки ж вільних валентностей (3 х II = 6) забезпечать три атома II-х валентного кисню. Вільних, невикористаних валентностей у атомів не залишилося. Значить, формула оксиду заліза (III) складена правильно: Fe2O3. Фактично, завдання зводиться до пошуку найменшого спільного кратного для валентностей двох елементів. Пояснимо це на ще одному прикладі. Напишемо формулу сполуки сірки (VI) з киснем:
Контролюючий блок №21. Наведіть приклади валентності таких хімічних елементів: водень, срібло, ртуть, берилій, кисень, свинець, алюміній, вуглець. Список джерел
Горбатко С. М. Гончар О. П. Зонков В.А.
|
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: