|
Гипермаркет знаний>>Химия>>Химия 9 класс>> Химия: Аминокислоты и белки
В этом параграфе мы рассмотрим важнейшие для всех живых организмов вещества, в состав которых, помимо углерода, водорода и кислорода, входит азот. Такие вещества участвуют в химических процессах, протекающих в организмах, и обеспечивают их жизнедеятельность. Это белки, продукты их расщепления в пищеварительном тракте — аминокислоты и многие витамины.
Начнем изучение азотсодержащих органических веществ с аминокислот. Их можно представить себе своеобразными кирпичиками, из которых строятся белки.
Как следует из самого слова "аминокислоты", эти вещества содержат характерную для органических кислот группу —СООН (вспомните, как называется эта группа) и еще одну характерную (функциональную) группу — аминогруппу —NH2.
Состав аминокислот можно выразить формулой:
NН2— СН —СООН
I
R
Аминокислоты можно рассматривать как производные кар-боновых кислот, у которых атом водорода в радикале замещен на аминогруппу. Например, из уксусной кислоты производится аминоуксусная кислота состава
NН2—СН2—СООН
На практике аминокислоты получают из карбоновых кислот, заместив в их радикале атом водорода на галоген, а затем галоген на аминогруппу при действии аммиака, например:

Карбоксильная группа -СООН в аминокислотах определяет их кислотные свойства.
Аминокислоты — это органические вещества, которые обладают одновременно кислотными основными свойствами, так как содержат амино- и карбоксильную группы.
Как вы знаете, такие вещества называются амфотерными (вспомните из курса неорганической химии свойства оксидов и гидроксидов переходных элементов, например Zn(ОН)2 и Аl(ОН)3).
Благодаря наличию кислотной и основной групп молекулы аминокислот способны взаимодействовать друг с другом и образовывать полимеры — белки.
Реакции получения полимеров, которые сопровождаются образованием побочного низкомолекулярного продукта, например воды, называются реакциями поликонденсации.
Как вы можете заметить из приведенного выше уравнения, при соединении молекул аминокислот друг с другом возникает связь.
Связь между остатком аминогруппы —NH— одной молекулы аминокислоты и остатком карбоксильной молекулы группы —СО— другой молекулы аминокислоты называется пептидной связью:
O H
| |
- CO - NH - или - C - N -
Эта связь повторяется в полимере много раз, и полимер соответственно называют полипептидом.
Как указано выше, из аминокислот строятся белки — полипептиды. Именно из белков путем их расщепления были получены многие аминокислоты. Исследователем, кто первым приступил к таким работам, был немецкий химик-органик Э. Г. Фишер.
Эмиль Герман Фишер (1852—1919)

Немецкий химик-органик и биохимик. Лауреат Нобелевской премии (1902). Научные работы посвящены химии углеводов, белков. Синтезировал ряд физиологически активных веществ. Внедрил в синтез химических соединений биокатализаторы — ферменты. Заслугой его является создание научной школы химиков-органиков.
Существует более 20 аминокислот, а белков — великое множество. Каждый организм на Земле имеет свой собственный неповторимый набор белков, который лишь иногда бывает сходен у близких родственников или одинаков у однояйцовых (идентичных) близнецов. Почему 20 аминокислот образуют бесчисленное белковое разнообразие? Чтобы понять, как это происходит, вспомните, что 33 буквы русского алфавита образуют огромное число слов. Еще более красноречив такой пример: в азбуке морзе знаков только два — точка и тире, и тем не менее с помощью их можно также передать все многообразие словарного запаса. Очевидно, вы поняли, что это многообразие определяется различной комбинацией букв.
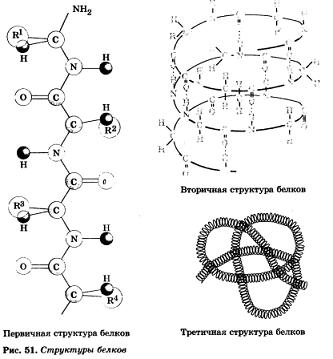
Аналогично и в молекулах белков порядок чередования аминокислот в полипептидной цепи определяет структуру белка. Эта структура называется первичной. Есть у белков и вторичная, и третичная структуры. С ними вы познакомитесь в курсе биологии. А здесь отметим, что большая заслуга в раскрытии строения белковой молекулы принадлежит русскому биохимику А. Я. Данилевскому.
Александр Яковлевич Данилевский
(1888—1923)

Русский биохимик. Один из основоположников отечественной биохимии. Работал в области химии ферментов и белков. В 1888 г. предложил теорию строения белковой молекулы. Экспериментально доказал, что действие сока поджелудочной железы на белки представляет собой гидролиз.
Белки выполняют в живом организме ряд очень важных функций.
Прежде всего, это строительная функция. Белки являются составной частью оболочки и цитоплазмы клеток и тем самым образуют все живые организмы.
Все биохимические реакции, идущие в клетках, протекают с помощью биологических катализаторов белковой природы — ферментов. Таким образом, белки выполняют каталитическую функцию.
Вспомните из курса анатомии человека, какие ферменты пищеварительных соков (слюны, желудочного и кишечного соков, сока поджелудочной железы) принимают участие в пищеварении. Какие особенности действия ферментов отличают их от неорганических катализаторов?
Еще одна очень важная функция белков — защитная. Особые белки — антитела (своеобразные наручники для проникающих в клетку преступников — бактерий, так как эти белки склеивают бактерии) и антитоксины (белки, которые нейтрализуют яды бактерий, образующиеся в результате их жизнедеятельности) определяют такое защитное свойство организмов, как иммунитет (вспомните из курса анатомии, что это за свойство).
Хорошо знакомый вам из курса анатомии белок крови — гемоглобин, который переносит кислород, выполняет транспортную функцию.
Запасающую, или энергетическую, функцию в клетках живых организмов несут особые белки. Например, богаты белками семена бобовых растений и яйцеклетки животных организмов. Энергия этих белков обеспечивает развитие нового организма.
Белки выполняют еще много важных функций: двигательную, сигнальную и т. д. Они могут превращаться в жиры и углеводы, но те, в свою очередь, превращаться в белки не могут. (Подумайте почему. Вспомните, в чем различие между этими веществами по составу.) Поэтому белковое голодание особенно опасно для живого организма.
Теперь перейдем к рассмотрению характерных для белков свойств.
Все белки способны гидролизоваться, т. е. разлагаться под действием кислот или щелочей с образованием аминокислот. Это свойство лежит в основе процесса пищеварения.
При некоторых воздействиях природная структура белка может разрушаться — как говорят, белок денатурируется. Это происходит даже при умеренном нагревании или изменении кислотности среды: растворимый в воде белок становится нерастворимым или свертывается. Каждый из вас наблюдал это явление при варке яиц (повышение температуры) и при скисании молока (изменение кислотности среды).
Белки горят, и этот процесс сопровождается появлением своеобразного запаха горящего рога (или жженого пера).
Для белков характерны цветные реакции, которые служат качественными на белки. Эти реакции, а также другие, характеризующие свойства белков, вы можете провести сами.
1. В пробирку налейте 2 мл раствора белка и прибавьте несколько капель концентрированной азотной кислоты. Образуется белый осадок. Нагрейте содержимое пробирки — осадок белка окрашивается в желтый цвет. Охладите смесь и добавьте осторожно, по каплям, концентрированный раствор аммиака (в избытке) — окраска становится оранжевой. Эта реакция называется ксантопротеиновой.
2. В пробирку налейте 2 мл раствора белка, добавьте столько же раствора щелочи и затем несколько капель разбавленного раствора медного купороса. Белок окрашивается в красно-фиолетовый цвет. Эта реакция называется биуретовой.
3. Немного хорошо измельченного мяса внесите в воду и прокипятите. После охлаждения жидкость отфильтруйте через вату и испытайте с помощью цветной реакции, содержится ли в растворе белок.
4. Подожгите несколько нитей какой-либо ткани и определите по запаху, какая это ткань: хлопчатобумажная или шерстяная.
5. Белки разнообразны по своему агрегатному состоянию: белки шерсти, шелка, ногтей, рога, перьев — нерастворимые волокна: белки крови, лимфы, пищеварительных соков — растворимы и образуют коллоидные растворы, из которых их можно осадить, приливая растворы солей тяжелых металлов (сульфата меди(II)), кислот (азотной, уксусной) или органических растворителей (спирта, ацетона). Используя белок куриного яйца, приготовьте в пробирке раствор белка и осадите его.
1. Аминокислоты и их амфотерность.
2. Получение аминокислот из карбоновых кислот.
3. Реакции поликонденсации.
4. Пептидная связь и полипептиды.
5. Первичная структура белков.
6. Биологические функции белков.
7. Свойства белков и качественные реакции на белки.
Почему аминокислоты являются веществами с двойственной функцией, т. е. имеют свойства двух разных классов веществ?
Чем отличается реакция поликонденсации от реакции полимеризации? В чем их сходство?
Что такое ферменты? Чем они отличаются от неорганических катализаторов?
Напишите уравнения реакций, с помощью которых можно осуществить следующие химические превращения:
этан —> этиловый спирт —» уксусный альдегид -> уксусная кислота хлоруксусная кислота —> аминоуксусная кислота —> полипептид (белок).
фотографии к уроку химии, химия 9 класс, шпаргалки для учеников
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|














