|
Гіпермаркет Знань>>Хімія>>Хімія 9 клас>> Тепловий ефект реакції. Екзотермічні та ендотермічні реакції. Термохімічне рівняння
ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕКЗОТЕРМІЧНІ ТА ЕНДОТЕРМІЧНІ РЕАКЦІЇ. ТЕРМОХІМІЧНЕ РІВНЯННЯ
Класифікація хімічних реакцій за тепловим ефектом. Термохімічне рівняння
• Тепловий ефект хімічної реакції - один із численних зовнішніх ефектів, що супроводжують перетворення одних речовин на інші. Завдання Назвіть інші зовнішні ефекти, які свідчать про перебіг хімічних реакцій. Унаслідок хімічних реакцій руйнуються зв'язки у вихідних речовинах (як їх називають?) і утворюються нові зв'язки, з'являються нові речовини (як їх називають?). Ці процеси супроводжуються виділенням або поглинанням енергії. Завдання 1. Наведіть приклади виділення або поглинання теплової енергії під час розчинення речовин у воді. 2. Установіть відповідність між співвідношеннями енергії Е', що витрачається на руйнування зв'язків між структурними частинками розчинюваної речовини та енергії E", яка виділяється під час утворення зв’язків між ними і частинками розчинника.
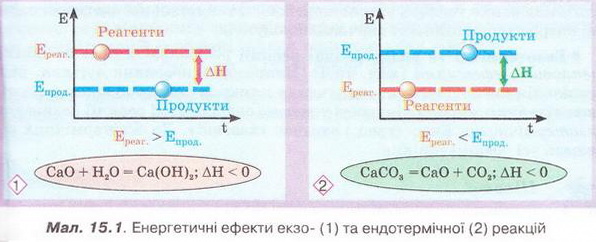
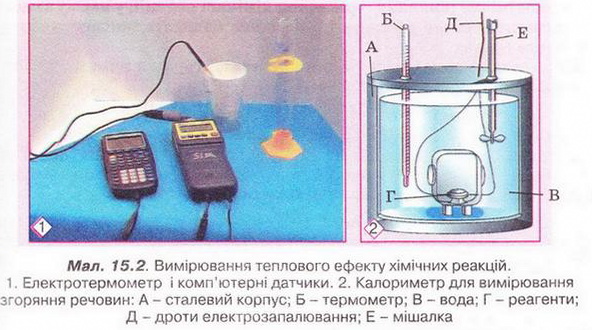
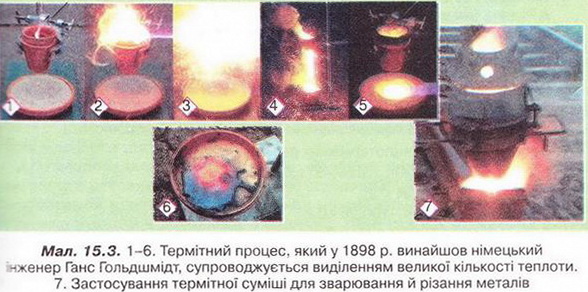
Чи можна стверджувати, що речовини ще до реакції мають певну енергію у «прихованій» формі? Спробуймо відповісти на це запитання. Вивчаючи природознавство та фізику, ви дізналися про хімічну, електричну, механічну, ядерну, сонячну форми існування енергії. Відповідно до різних форм енергії по-різному виявляються й енергетичні ефекти. хімічних реакцій. Пригадаймо, розкласти воду на водень і кисень можна електролізом. Потрібна для цього електрична енергія виділяється внаслідок перебігу окисно-відновних реакцій під час роботи акумулятора. Згоряння магнію супроводжується виділенням теплової та світлової енергії. А розкладання хлориду й броміду Аргентуму(І) у фотографічному процесі відбувається з поглинанням світлової енергії. Також унаслідок перебігу хімічних реакцій може виконуватись механічна робота - наприклад, під час вибуху або роботи двигуна внутрішнього згоряння. Усі ці факти доводять існування внутрішньої енергії, яка «прихована» в речовинах і вивільняється під час хімічних процесів. Тобто хімічні х акції супроводжуються зміною не тільки складу й будови речовин, а й зміною їхньої внутрішньої енергії. Енергію, виділену або поглинуту системою під час перебігу в ній хімічної реакції, називають енергетичним ефектом реакції. Він становить різницю між внутрішньою енергією реагентів і продуктів реакції (мал. 15.1). Часто внаслідок перетворення одних речовин на інші виділяється або поглинається теплова енергія. її кількість (позначають ΔН, вимірюють у Дж, кДж тощо) називають тепловим ефектом хімічної реакції. Він залежить від природи реагуючих речовин, їхньої кількості та агрегатного стану, тиску тощо. Тому з метою стандартизації теплові ефекти зазначають для температури 25 °С і тиску 0,101 мПа. Теплові ефекти визначають експериментально (мал. 15.2) в спеціальних приладах - калориметрах. На практиці обчислюють теплові ефекти для оцінювання теплоти згоряння речовин, теплотворної здатності палива, енергетичної цінності харчових продуктів. • Екзотермічні та ендотермічні реакції розрізняють саме за їхніми тепловими ефектами (мал. 15.1). Наприклад, згоряння вугілля, нейтралізація кислот лугами, сполучення цинку із сіркою супроводжуються виділенням значної кількості теплової енергії. Такі реакції називають екзотермічними. Екзо- (грец.) означає «назовні». До екзотермічних належать усі реакції горіння. Цікаво? Уперше перебіг реакції цинку із сіркою дослідив і описав шведський хімік Георг Брандт. Він змішав тонко подрібнені сірку масою 1 г та цинк масою 2 г, а потім торкнувся суміші розпеченим сталевим шпателем. Спалахнуло полум'я, з'явився густий білий дим. Пізнавально! Перебіг реакцій термічного розкладання кальцій карбонату, калій перманганату, малахіту потребує безперервного надходження теплової енергії ззовні. За відсутності нагрівання ці реакції негайно припиняються, їх називають ендотермічними. Ендотермічна реакція: реагенти + теплова енергія → продукти. Екзотермічна реакція: реагенти → продукти + теплова енергія. Чимало реакцій розкладу - ендотермічні, однак поміж них трапляються й екзотермічні. Визначмо, екзо- чи ендотермічною реакцією є розкладання амоній дихромату (про це йшлося у § 13) - так званий вулкан Беттгера. Аби розпочалася реакція, сполуку нагрівають - торкаються запаленою скіпкою чи розпеченою скляною паличкою. Подальший інтенсивний перебіг реакції не потребує нагрівання й супроводжується виділенням чималої кількості теплової й світлової енергії. Ця реакція - екзотермічна. Про науковця, який запровадив поняття «екзо-» та «ендотермічні реакції», ви дізнаєтеся з підпису до малюнка 18.4. Термохімічне рівняння - рівняння хімічної реакції, у якому зазначають агрегатні стани речовин і для якого наводять числове значення теплового ефекту. Наприклад, термохімічне рівняння реакції горіння метану - головно: складової природного газу - таке: СН4(г) +202(г) = С02(г) + 2Н20(р); ΔН = -890 кДж, де (г) - газ, (р) - рідина. Тверду речовину позначають (т). Тепловий ефект відповідає тій кількості метану, яка визначені рівнянням реакції, - 1 моль. А тепловий ефект неповного згоряння графіту зазначено для речовини кількістю 2 моль: 2С(графіт) + O2(г) = 2СО(г); ΔН = -221 кДж. Завдання Прокоментуйте термохімічне рівняння окиснення нітроген(ІІ) оксиду: N2(Г) + O2(г) = 2NO(Г); ΔН = 280 кДж. Якщо агрегатні стани учасників реакції очевидній не потребують уточнень, то ці відомості у термохімічному рівнянні можна не зазначати. Тож трапляються й спрощені записи термохімічних рівнянь: СН4 + 2O2 = СO2 + 2Н2O; ΔН < 0 За ними також можна класифікувати хімічні реакції на екзо- та ендотермічні, але вони не дають уявлення про числове значення теплового ефекту. Завдання Класифікуйте хімічні реакції за тепловим ефектом: • Значення теплових ефектів, якими супроводжуються хімічні реакції важко переоцінити. Екзотермічні реакції використовують у промисловості та побуті для вироблення енергії, одержання високотемпературного полум'я, видобування металів. Наприклад, у реакції ферум(ІІІ) оксиду з алюмінієм. Fе2O3 + 2Аl = 2Fе + Аl2O3; ΔН < O (так званий термітний процес) унаслідок виділення великої кількості теплової енергії температура сягає 2400 °С, тому залізо плавиться (мал. 15.3). Завдання Розгляньте термітний процес з точки зору окиснення-відновлення. На ендотермічних процесах ґрунтуються промислові й лабораторні способи добування неорганічних і органічних сполук, їх використовують у лабораторній практиці, побуті, медицині для швидкого охолодження лив. § 5). Стисло про головне Унаслідок хімічних реакцій руйнуються зв'язки у реагентах і утворюються нові зв'язки, з'являються нові речовини - продукти реакції. Ці процеси супроводжуються виділенням або поглинанням енергії. Хімічні реакції супроводжуються не тільки зміною складу та будови речовин, а й зміною їхньої внутрішньої енергії. Енергію, виділену або поглинуту системою під час перебігу в ній хімічної реакції, називають енергетичним ефектом реакції. Він становить різницю між внутрішньою енергією реагентів і продуктів реакції. Часто внаслідок перетворення одних речовин на інші виділяється або поглинається теплота. її кількість (позначають ΔН, вимірюють у Дж, кДж тощо) називають тепловим ефектом хімічної реакції. Екзотермічні та ендотермічні реакції розрізняють саме за їхніми тепловими ефектами. Екзотермічні реакції супроводжуються виділенням теплоти, а ендотермічні - поглинанням теплової енергії. Термохімічне рівняння - рівняння хімічної реакції, у якому зазначають агрегатні стани речовин і для якого наводять числове значення теплового ефекту. Тепловий ефект відповідає тій кількості речовини, яка визначена рівнянням реакції. Екзо- та ендотермічні реакції широко використовують у промисловості та побуті. Поміж обмінних процесів у живих організмах є як екзо-, так і ендотермічні реакції. Застосуйте свої знання й уміння 1. Назвіть енергетичні ефекти, які можуть супроводжувати перебіг хімічних реакцій. 2. Поясніть, чому під час перебігу хімічних реакцій обов'язково виділяється або поглинається енергія. 3. Наведіть приклади екзо- та ендотермічних реакцій. 4. Виберіть правильне твердження. Енергетичний ефект реакції дорівнює: А Різниці між внутрішньою енергією реагентів і продуктів реакції; Б Добутку внутрішньої енергії реагентів і продуктів реакції; В Сумі внутрішніх енергій-реагентів і продуктів реакції; Г Відношенню внутрішніх енергій реагентів продуктів реакції. 5. Виберіть одиниці виміру теплового ефекту хімічної реакції: 6. Поясніть, чим термохімічне рівняння відрізняється від хімічного. 7. Виберіть рівняння ендотермічних реакцій A 2H2(Г) + O2(Г) = 2H2O(p); ΔH = -571,6 кДж; 8. Аби виготовити хімічну грілку, у мішечок з водонепроникного матеріалу вміщують суміш купрум(ІІ) хлориду, порошку алюмінію та наповнювача (деревні ошурки). Після добавляння води відбувається хімічна реакція, яка супроводжується виділенням теплової енергії. Поясніть, чому реакція відбувається лише після добавляння води. Класифікуйте цю реакцію за тепловим ефектом, запишіть її термохімічне рівняння. 9. Запишіть два рівняння реакції нейтралізації у повній і скороченій йонній формах. Поясніть, у чому полягає суть реакції нейтралізації. Висловіть припущення, чому всі реакції нейтралізації мають приблизно однаковий тепловий ефект. 10. Проаналізуйте зміст третьої колонки таблиці 13.1 і визначте, про що ви дізналися і чого навчилися, опрацювавши § 15.
Повний перелік тем з хімії, календарний план по всім предметам згідно шкільної програми, домашня робота, курси та завдання з хімії для 9 класу
Зміст уроку
Если у вас есть исправления или предложения к данному уроку, напишите нам. Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум. |
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: