|
Гіпермаркет Знань>>Хімія>>Хімія 10 клас>> Практичні роботи: 1. Добування вуглекислого газу. Взаємоперетворення карбонатів і гідрогенкарбонатів
Практична робота 1
Добування аміакуі дослід з ним
Коротка інструкція:
1. Зберіть прилад, як показано на мал. 7, с. 50.
2. Приготуйте суміш приблизно рівних порцій (по половині чайної ложки) кристалічного хлориду амонію і порошку гідроксиду кальцію.
3. Насипте суміш у суху пробірку на 1/3 її об'єму і закрийте пробкою з відвідною трубкою, зігнутою під прямим кутом і повернутою отвором догори (чому?).
4. Пробірку з сумішшю затисніть у лапці штатива трохи похило, отвором донизу. На кінець відвідної трубки надіньте догори дном суху пробірку і легко закрийте її отвір жмутиком вати.
5. Обережно прогрійте спочатку всю пробірку, а потім нагрівайте в тому місці, де є суміш.
6. Як тільки відчуєте гострий запах аміаку (нюхати обережно!), пробірку, в яку зібрано аміак, обережно зніміть з відвідної трубки, тримаючи її догори дном, негайно закрийте отвір великим пальцем і опустіть у кристалізатор з водою (кінець газовідвідної трубки після зняття з неї пробірки з аміаком відразу закрийте жмутиком мокрої вати).
7. Коли пробірка, в яку збирали аміак, заповниться водою, знову закрийте її отвір великим пальцем під водою і вийміть з кристалізатора.
8. Добутий водний розчин аміаку поділіть на дві пробірки. В одну занурте червоний лакмусовий папірець, а в іншу — долийте кілька крапель фенолфталеїну, а потім — трохи розбавленої хлоридної кислоти. Що спостерігається?
Запитання і завдання
1. Чому пробірку з сумішшю треба закріплювати в лапці штатива похило у бік отвору?
2. Чому аміак збирають у суху пробірку, перевернену догори дном?
3. Про які властивості водного розчину аміаку свідчить його дія на індикатори?
4. Як це можна пояснити на підставі уявлень про електролітичну дисоціацію?
5. Що відбувається при дії на водний розчин аміаку кислотою?
6. Напишіть, де можливо, рівняння реакцій у молекулярній, повній і скороченій йонних формах.
Практична робота 2
Добування оксидукарбону(IV), взаємоперетворення карбонатів і гідрокарбонатів
Коротка інструкція:
1. У пробірку покладіть кілька шматочків крейди або мармуру і долийте трохи розбавленої хлоридної кислоти.
2. Пробірку швидко закрийте корком з відвідною трубкою, кінець якої занурте у пробірку з вапняною водою (1 — 2 мл). Що спостерігається?
3. Продовжуйте пропускати газ у цю саму пробірку доти, доки не зникне каламуть і утвориться прозорий розчин.
Запитання і завдання
1. Що відбувається при дії хлоридної кислоти на карбонати?
2. Як двома способами довести, що з пробірки виділяється саме оксид карбону(IV)?
3. Як пояснити появу каламуті в пробірці з вапняною водою, крізь яку пропускали оксид карбону(IV), і розчинення каламуті?
4. Напишіть рівняння реакцій у молекулярній, повній і скороченій йонних формах.
Практична робота З
Розв'язування експериментальних задач
Завдання:
1. Визначити, яка речовина міститься в кожній з чотирьох пробірок (кристалічні речовини):
Варіант 1 — сульфат натрію, карбонат кальцію, гідроксид кальцію, хлорид кальцію;
Варіант 2 — карбонат натрію, сульфат натрію, сульфіт натрію, хлорид натрію.
2. Написати рівняння реакцій у молекулярній, повній і скороченій йонних формах.
3. Здійснити реакції, що виражаються такими йонними рівняннями:
Варіант І: а) 2Н+ + СО2-3 → CO2↑ + Н20
б) Са2+ + СО2-3 → СаС03↓
Варіант 2: а) Са2+ + 2НСО-3 → СаС03↓ + Н20
б) Са2+ + SiO2-3 → СаSіОз↓
4. Написати рівняння реакцій у молекулярній формі.
Практична робота 4
Виявлення Карбону, Гідрогену, Хлору в органічних речовинах
Дослід 1. Виявлення Карбону і Гідрогену.
Суміш досліджуваної речовини з оксидом купруму (ІІ) помістіть у суху пробірку і закріпіть її у штативі у горизонтальному положенні (мал. 33). Обережно внесіть безводний сульфат купруму (ІІ) і закрийте пробірку корком з газовідвідною трубкою, кінець якої опустіть у пробірку з вапняною водою.
Обережно нагрівайте пробірку з досліджуваною речовиною. Спостерігайте зміни, що відбулися з оксидом купруму (ІІ), сульфатом купруму (ІІ), вапняною водою; після цього дослід припиніть.
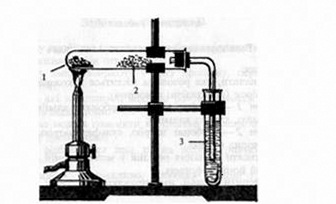
Мал. 33. Виявлення Карбону і Гідрогену в органічній сполуці:
1 — суміш речовини, що досліджується, з оксидом купруму(ІІ);
2 — безводний сульфат купруму (ІІ); 3 — вапняна вода
З метою уникнення розтріскування пробірки стежте, щоб після припинення нагрівання рідина не перекидалася по трубці у прилад.
Запитання і завдання
1. Яку роль відіграє в даному досліді оксид купруму (ІІ)?
2. З якою метою використовується вапняна вода?
3. Напишіть рівняння реакцій, що відбуваються.
Дослід 2. Виявлення хлору.
Кінець мідного дроту зігніть петелькою або у вигляді спіралі діаметром 1—2 мм. Прожарюйте дротину в полум'ї до тих пір, поки воно не перестане забарвлюватись, охолодіть її. Внесіть дротину в речовину, що досліджується, і знову в полум'я (мал. 34).
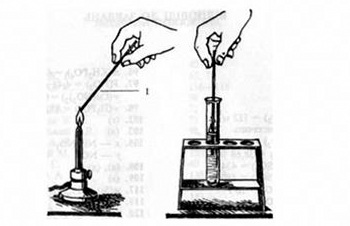
Зелене забарвлення полум'я свідчить про наявність хлору в сполуці, виданій для аналізу. Ємності з легкозаймистими органічними сполуками тримайте далі від вогню.
Н.М. Буринська, Л.П. Величко, Хімія, 10 клас
Вислано читачами з інтернет-сайтів
Збірка конспектів уроків по всім класами, домашня робота, скачати реферати з хімії, книги та підручники згідно каленадарного плануванння з хімії для 10 класу
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|












