|
Гипермаркет знаний>>Химия>>Химия 8 класс>> Химия: Изменения в составе ядер атомов химических элементов. Изотопы
Итак, мы выяснили, что атом — мельчайшая частица химического элемента — оказался сложным и уникальным образо ваннем природы, построенным из трех видов элементарных частиц — протонов, нейтронов и электронов.
Положение химического элемента в Периодической системе Д. И. Менделеева зависит от величины заряда ядра атома, то есть от числа протонов в нем. Попробуем представить себе, что будет, если изменить число протонов в ядре, то есть заряд атомного ядра. Конечно же получатся на исходного элемента совсем другие химические элементы. Такие процессы называются ядерными и происходят, например, на Солнце, где ядра атомов водорода соединяются и образуют ядра атомов гелия. Эти процессы протекают с выделением огромного количества энергии. Подобные процессы человек научился проводить и на Земле. Мечта алхимиков о превращении неблагородных элементов в золото стили возможной. Но чтобы эти процессы протекали, нужно затратить громадную энергию, и такое золото будет стоить в сотни раз дороже добываемого обычными способами.
Теперь, если, не менян число протонов в атоме химического элемента, то есть заряд ядра, изменить число нейтронов, то логично пред пол ожить, что положение химического элемента в Периодической системе не изменится, то есть из исходного химического элемента не образуется нового элемента. Это будет все тот же химический элемент, но атомы его будут отличаться от исходных своей массой.
Химический элемент — зто совокупность атомов с одинаковым зарядом ядра.
1. Ядерные процессы. 2. Превращения элемента. 8. Изотопы. 4. Изотопы водорода.
Разновидности атомов одною и того же химического злемента, имеющие одинаковый заряд ядра, но ралное массовое число, называются изотопами.
Слово изотоп состоит из двух греческих стон: изое — «один» и топос — «место», обозначает «занимающий одно место» (клетку) в Периодической системе элементов.
Химические элементы, встречающиеся в природе, являются смесью изотопов. Так, углерод имеет три изотопа с массой 12, 13 и 11; кислород — три изотопа с массой 16,17 и 18 и т. д.
Обычно приводимая в Периодической системе относительная атомная масса химического элемента является средним значением атомных масс природной смеси изотопов данного элемента с учетом их относительного содержания в природе, поэтому их значения довольно часто имеют дробные значения. Например, атомы природного хлора представляют собой смесь двух изотопов с массой 35 (их в природе 75%) и 37 (их 25% ); следовательно, относительная атомная масса хлора равна 35,5. Изотопы хлора записываются так:

Химические свойства изотопов хлора совершенно одинаковы, как и изотопов большинства химических элементов, например калия, аргона:


Почему в Периодической системе Д. И. Менделеев относительная атомная масса аргона близка к 40, а калия — к 39?
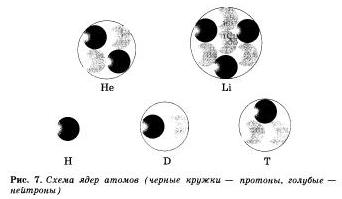
Почему изотопы хлора одинаковы между собой по свойствам, тогда как изотопы водорода разнятся?
Почему дейтерневую воду D20 называют тяжелой водой? Приготовьте сообщение «Сравнение свойств легкой и тяжелой воды», пользуясь дополнительной литературой.
Найдите в Периодической системе химических элементов три пары элементов, у которых подобно паре Аr — К вначале расположен элемент с большом значением относительной атомной массы.
учебники по всем предметам, видео для 8 класса, конспекты уроков химии и физики
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|












