|
|
|
| Строка 3: |
Строка 3: |
| | <br> <metakeywords>Хімія, клас, урок, на тему, 9 клас, Гомологи метану, їх Фізичні властивості, Молекулярні та структурні формули, назви, Моделі молекул, Значення моделювання в хімії.</metakeywords>ГОМОЛОГИ МЕТАНУ. ФІЗИЧНІ ВЛАСТИВОСТІ ГОМОЛОГІВ МЕТАНУ. МОЛЕКУЛЯРНІ ТА СТРУКТУРНІ ФОРМУЛИ, НАЗВИ. МОДЕЛІ МОЛЕКУЛ. ЗНАЧЕННЯ МОДЕЛЮВАННЯ В ХІМІЇ | | <br> <metakeywords>Хімія, клас, урок, на тему, 9 клас, Гомологи метану, їх Фізичні властивості, Молекулярні та структурні формули, назви, Моделі молекул, Значення моделювання в хімії.</metakeywords>ГОМОЛОГИ МЕТАНУ. ФІЗИЧНІ ВЛАСТИВОСТІ ГОМОЛОГІВ МЕТАНУ. МОЛЕКУЛЯРНІ ТА СТРУКТУРНІ ФОРМУЛИ, НАЗВИ. МОДЕЛІ МОЛЕКУЛ. ЗНАЧЕННЯ МОДЕЛЮВАННЯ В ХІМІЇ |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | <u>Гомологи метану. Молекулярні та структурні формули, назви.</u><br> | + | <u>Гомологи метану. Молекулярні та структурні формули, назви.</u><br> |
| | | | |
| - | Після опрацювання § 22 ви зможете:<br> | + | Після опрацювання § 22 ви зможете:<br> |
| | | | |
| - | називати перші 10 членів гомологічного ряду метану, загальну формулу цього ряду; складати молекулярні, електронні та структурні формули гомологів метану й пояснювати їх; збирати моделі молекул гомологів метану; пояснювати суть гомології.<br> | + | називати перші 10 членів гомологічного ряду метану, загальну формулу цього ряду; складати молекулярні, електронні та структурні формули гомологів метану й пояснювати їх; збирати моделі молекул гомологів метану; пояснювати суть гомології.<br> |
| | | | |
| - | На шляху до успіху пригадаємо з вивчених курсів хімії:<br> | + | На шляху до успіху пригадаємо з вивчених курсів хімії:<br> |
| | | | |
| - | що таке кристалогідрати; як визначають карбон (IV) оксид; яку будову має молекула метану; як складають електронні формули речовин; що таке спрощена структурна формула і як її перетворити на повну структурну формулу речовини.<br> | + | що таке кристалогідрати; як визначають карбон (IV) оксид; яку будову має молекула метану; як складають електронні формули речовин; що таке спрощена структурна формула і як її перетворити на повну структурну формулу речовини.<br> |
| | | | |
| - | • ''Гомологи метану ''(алкани) трапляться у нашому житті чи не на кожному кроці (мал. 22.1). Вони - компоненти природного і попутного нафтового газу, нафти.<br> | + | • ''Гомологи метану ''(алкани) трапляться у нашому житті чи не на кожному кроці (мал. 22.1). Вони - компоненти природного і попутного нафтового газу, нафти.<br> |
| | | | |
| - | Що означає слово «гомолог»? У перекладі з давньогрецької [[Image:Chemistry_147_2.jpg]] означає «подібний, схожий», а [[Image:Chemistry_147_3.jpg]] - «слово», «закон». Чим саме подібні до метану та між собою його гомологи?<br>
| + | [[Image:Chemistry_147.jpg]] |
| | | | |
| - | Елементний склад численних гомологів метану з'ясуймо за допомогою простого досліду (мал. 22.2). Продукти згоряння парафіну пропустімо послідовно через безводний купрум(ІІ) сульфат і водний розчин кальцій гідроксиду (вапняну воду).<br>
| + | Що означає слово «гомолог»? У перекладі з давньогрецької [[Image:Chemistry 147 2.jpg]] означає «подібний, схожий», а [[Image:Chemistry 147 3.jpg]] - «слово», «закон». Чим саме подібні до метану та між собою його гомологи?<br> |
| | | | |
| - | Помутніння вапняної води зумовлює продукт повного окиснення парафіну карбон(IV) оксид. Його утворення під час горіння парафіну є підставою стверджувати, що у складі гомологів метану є Карбон. Кіптява, яка утворюється під час неповного згоряння парафіну, також свідчить про наявність Карбону у складі його компонентів.<br>
| + | Елементний склад численних гомологів метану з'ясуймо за допомогою простого досліду (мал. 22.2). Продукти згоряння парафіну пропустімо послідовно через безводний купрум(ІІ) сульфат і водний розчин кальцій гідроксиду (вапняну воду).<br> |
| | | | |
| - | <u>''Завдання''</u><br>
| + | [[Image:Chemistry_147_1.jpg]] |
| | | | |
| - | Запишіть рівняння реакції між карбон(IV) оксидом і кальцій гідроксидом. Класифікуйте цю хімічну реакцію.<br>
| + | Помутніння вапняної води зумовлює продукт повного окиснення парафіну карбон(IV) оксид. Його утворення під час горіння парафіну є підставою стверджувати, що у складі гомологів метану є Карбон. Кіптява, яка утворюється під час неповного згоряння парафіну, також свідчить про наявність Карбону у складі його компонентів.<br> |
| | | | |
| - | Другий продукт повного окиснення парафіну - вода. Отже, до складу гомологів метану входить Гідроген.<br>
| + | <u>''Завдання''</u><br> |
| | | | |
| - | ''<u>Завдання</u>''<br>
| + | Запишіть рівняння реакції між карбон(IV) оксидом і кальцій гідроксидом. Класифікуйте цю хімічну реакцію.<br> |
| | | | |
| - | Опишіть зміну кольору безводного купрум(ІІ) сульфату (мал. 22.2). Запишіть хімічне рівняння, яке пояснює ці зміни (див. § 5).<br>
| + | Другий продукт повного окиснення парафіну - вода. Отже, до складу гомологів метану входить Гідроген.<br> |
| | | | |
| - | Якісний і кількісний аналіз довели, що будь-який гомолог метану містить лише два хімічні елементи - Карбон і Гідроген. Такі речовини називають вуглеводнями. Однак не всі вуглеводні є гомологами метану. До них належать лише ті, склад яких описує загальна формула С<sub>n</sub>Н<sub>2n</sub><sub>+2</sub>, де n - додатне ціле число. Наприклад, молекулярна формула алкану, у складі якого 4 атоми Карбону, - С<sub>4</sub>Н<sub>10</sub>.<br>
| + | ''<u>Завдання</u>''<br> |
| | | | |
| - | ''<u>Завдання</u>'''''<i><u><br></u></i>'''''<u></u>''
| + | Опишіть зміну кольору безводного купрум(ІІ) сульфату (мал. 22.2). Запишіть хімічне рівняння, яке пояснює ці зміни (див. § 5).<br> |
| | | | |
| - | Запишіть молекулярні формули алканів, у складі яких: а) 2; б) 5; в) 17 атомів Карбону.<br>
| + | Якісний і кількісний аналіз довели, що будь-який гомолог метану містить лише два хімічні елементи - Карбон і Гідроген. Такі речовини називають вуглеводнями. Однак не всі вуглеводні є гомологами метану. До них належать лише ті, склад яких описує загальна формула С<sub>n</sub>Н<sub>2n</sub><sub>+2</sub>, де n - додатне ціле число. Наприклад, молекулярна формула алкану, у складі якого 4 атоми Карбону, - С<sub>4</sub>Н<sub>10</sub>.<br> |
| | | | |
| - | Отже, поміж розмаїття органічних сполук можна виокремити речовини з однаковим якісним складом, подібні за будовою і хімічними властивостями. Такі речовини називають гомологами. За кількісним складом вони відрізняються один від одного на певну кількість груп -СН<sub>2</sub>-. Групу -СН<sub>2</sub>- називають гомологічною різницею. Гомологи, розташовані за зростанням їхньої відносної молекулярної маси, утворюють гомологічний ряд. Формула будь-якого наступного гомолога може бути отримана додаванням гомологічної різниці до формули попереднього члена гомологічного ряду.<br>
| + | ''<u>Завдання</u>'''''<i><u><br></u></i>'''''<u></u>'' |
| | | | |
| - | <u>''Завдання''</u><br>
| + | Запишіть молекулярні формули алканів, у складі яких: а) 2; б) 5; в) 17 атомів Карбону.<br> |
| | | | |
| - | Поясніть, як, знаючи хімічну формулу гексану С<sub>6</sub>Н<sub>14</sub>, визначити формулу гомолога, який у гомологічному ряду: а) передує йому; б) розташований після нього.<br>
| + | Отже, поміж розмаїття органічних сполук можна виокремити речовини з однаковим якісним складом, подібні за будовою і хімічними властивостями. Такі речовини називають гомологами. За кількісним складом вони відрізняються один від одного на певну кількість груп -СН<sub>2</sub>-. Групу -СН<sub>2</sub>- називають гомологічною різницею. Гомологи, розташовані за зростанням їхньої відносної молекулярної маси, утворюють гомологічний ряд. Формула будь-якого наступного гомолога може бути отримана додаванням гомологічної різниці до формули попереднього члена гомологічного ряду.<br> |
| | | | |
| - | Зауважмо, що гомологічні ряди можна побудувати для всіх класів органічних сполук. Приміром, на схемі 22.1 зазначено назви деяких органічних речовин, з якими ви ознайомитеся цього року. Кожна зі сполук є представником певного гомологічного ряду. Проте не обов'язково докладно вивчати усі представники ряду. Адже знаючи властивості одне: і з членів гомологічного ряду, можна дійти висновків щодо властиве і інших представників того ж ряду. Це й зумовлює важливість поняття гомології під час вивчення органічної хімії.<br>
| + | <u>''Завдання''</u><br> |
| | | | |
| - | • ''Молекулярні та структурні формули, назви'' перших десяти членів гомологічного ряду метану представлені у таблиці 22.1. Зверніть увагу на наведені у ній повні структурні формули алканів: кожний наступні гомолог метану виведено з попереднього. Це може бути зроблено заміщенням на групу -СН<sub>3</sub> одного з атомів Гідрогену або розташуванням групи -СН<sub>2</sub>- між двома сусідніми атомами Карбону (мал. 22.3).<br>
| + | Поясніть, як, знаючи хімічну формулу гексану С<sub>6</sub>Н<sub>14</sub>, визначити формулу гомолога, який у гомологічному ряду: а) передує йому; б) розташований після нього.<br> |
| | | | |
| - | <u>''Завдання''</u><br>
| + | Зауважмо, що гомологічні ряди можна побудувати для всіх класів органічних сполук. Приміром, на схемі 22.1 зазначено назви деяких органічних речовин, з якими ви ознайомитеся цього року. Кожна зі сполук є представником певного гомологічного ряду. Проте не обов'язково докладно вивчати усі представники ряду. Адже знаючи властивості одне: і з членів гомологічного ряду, можна дійти висновків щодо властиве і інших представників того ж ряду. Це й зумовлює важливість поняття гомології під час вивчення органічної хімії.<br> |
| | | | |
| - | Виведіть двома способами структурну формулу гептану зі структурної формули гексану.<br>
| + | • ''Молекулярні та структурні формули, назви'' перших десяти членів гомологічного ряду метану представлені у таблиці 22.1. Зверніть увагу на наведені у ній повні структурні формули алканів: кожний наступні гомолог метану виведено з попереднього. Це може бути зроблено заміщенням на групу -СН<sub>3</sub> одного з атомів Гідрогену або розташуванням групи -СН<sub>2</sub>- між двома сусідніми атомами Карбону (мал. 22.3).<br> |
| | | | |
| - | <u>''Завдання''</u><br>
| + | [[Image:Chemistry_149.jpg]] |
| | | | |
| - | 1. Запишіть електронні формули пропану та пентану. 2. Проаналізуйте зміст таблиці 22.1 і визначте, чи справедливі загальні закономірності зміни кількісного складу гомологів для представників гомологічного ряду метану.<br>
| + | [[Image:Chemistry_149_1.jpg]] |
| | | | |
| - | Повні структурні формули відображують послідовність розміщення атомів Карбону і Гідрогену. З них очевидно, що в алканах атоми Карбону сполучені між собою тільки одинарними (простими, ординарними) зв'язками, а решта зв'язків з'єднує їх з атомами Гідрогену. Аби з'ясувати, як атоми Карбону і Гідрогену розміщені один відносно одного у просторі, звернімося до матеріальних моделей алканів (мал. 22.4).<br>
| + | [[Image:Chemistry_150.jpg]] |
| | | | |
| - | У метані та його гомологах зв'язки між атомами розміщені в просторі під кутом 109,5°. Тому молекула найпростішого алкану має тетраедричну форму, у молекулі етану два атоми Карбону розташовані на одній прямій, а молекули решти алканів набувають зигзагуватої форми (мал. 22.5).<br>
| + | <u>''Завдання''</u><br> |
| | | | |
| - | <u>''Завдання''</u><br>
| + | Виведіть двома способами структурну формулу гептану зі структурної формули гексану.<br> |
| | | | |
| - | За спрощеними структурними формулами деяких алканів запишіть їхні повні структурні й електронні формули:<br>
| + | <u>''Завдання''</u><br> |
| | | | |
| - | Починаючи від етану виникає живість обертання навколо ординарного зв'язку С - С. Внаслідок цього молекули алканів можуть набувати різноманітних геометричних форм (мал. 22.4, 4, а - г). Молекулам алканів з понад двома атомами Карбону в ланцюзі властиві вигнуті форми.<br>
| + | 1. Запишіть електронні формули пропану та пентану. 2. Проаналізуйте зміст таблиці 22.1 і визначте, чи справедливі загальні закономірності зміни кількісного складу гомологів для представників гомологічного ряду метану.<br> |
| | | | |
| - | Найміцніше засвоюється інформація, одержувана під час самостійного спостереження або дослідження. Аби на власні очі (радше сказати, власноруч) пересвідчитися у зигзагуватій будові карбонового ланцюга і можливостях обертання атомів навколо карбон-карбонових зв’язків, виконайте лабораторний дослід.<br>
| + | Повні структурні формули відображують послідовність розміщення атомів Карбону і Гідрогену. З них очевидно, що в алканах атоми Карбону сполучені між собою тільки одинарними (простими, ординарними) зв'язками, а решта зв'язків з'єднує їх з атомами Гідрогену. Аби з'ясувати, як атоми Карбону і Гідрогену розміщені один відносно одного у просторі, звернімося до матеріальних моделей алканів (мал. 22.4).<br> |
| | | | |
| - | ЛАБОРАТОРНИЙ ДОСЛІД<br>
| + | [[Image:Chemistry_151.jpg]] |
| | | | |
| - | ''№ 6. Виготовлення моделей молекул вуглеводнів''<br> | + | У метані та його гомологах зв'язки між атомами розміщені в просторі під кутом 109,5°. Тому молекула найпростішого алкану має тетраедричну форму, у молекулі етану два атоми Карбону розташовані на одній прямій, а молекули решти алканів набувають зигзагуватої форми (мал. 22.5).<br> |
| | | | |
| - | Завдання. Виготовте моделі молекул метану, етану, пропану, бутану, пентану та підготуйте план складання моделей.<br>
| + | [[Image:Chemistry_151_1.jpg]] |
| | | | |
| - | Обладнання: пластилін темного і світлого кольорів, сірники або набір для складання кулестержневих моделей молекул.<br>
| + | <u>''Завдання''</u><br> |
| | | | |
| - | Порада. Об'єднайтеся в «домашні» групи з п'ятьох учнів, ознайомтеся із завданням: кожен з вас має вибрати вуглеводень, який моделюватиме. Перейдіть до «робочої» групи - усі її члени виготовлятимуть модель одного й того самого вуглеводню. Ви зможете порівняти з роботами інших учнів власноруч виготовлену модель та разом скласти план її виготовлення. Потім поверніться до своєї «домашньої» групи, аби продемонструвати свій доробок і узагальнити здобуті знання та вміння. Порівняйте готові моделі і складені плани, виокремте ті пункти плану, які можна використати для самоконтролю.<br>
| + | За спрощеними структурними формулами деяких алканів запишіть їхні повні структурні й електронні формули:<br> |
| | | | |
| - | Інструкції для «робочих» груп<br>
| + | [[Image:Chemistry_151_2.jpg]] |
| | | | |
| - | Інструкція 1. Змоделюйте молекулу метану. Для цього зі світлого пластиліну виготовте чотири кульки діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - одну кульку, діаметр якої в 1,5 раза більший за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену й Карбону. На поверхні моделі атома Карбону позначте чотири рівновіддалені по кутах тетраедра точки. Вставте в них сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі метану? Перевірте чи дорівнюють кути між зв'язками 109,5°. Підготуйте план складання моделі цієї молекули.<br>
| + | Починаючи від етану виникає живість обертання навколо ординарного зв'язку С - С. Внаслідок цього молекули алканів можуть набувати різноманітних геометричних форм (мал. 22.4, 4, а - г). Молекулам алканів з понад двома атомами Карбону в ланцюзі властиві вигнуті форми.<br> |
| | | | |
| - | Інструкція 2. Змоделюйте молекулу етану. Для цього зі світлого пластиліну виготовте шість кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - дві кульки, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок - моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедрі точки. Обидві кульки з'єднайте сірником. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі етану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. Підготуйте план складання моделі цієї молекули.<br>
| + | Найміцніше засвоюється інформація, одержувана під час самостійного спостереження або дослідження. Аби на власні очі (радше сказати, власноруч) пересвідчитися у зигзагуватій будові карбонового ланцюга і можливостях обертання атомів навколо карбон-карбонових зв’язків, виконайте лабораторний дослід.<br> |
| | | | |
| - | Інструкція 3. Змоделюйте молекулу пропану. Для цього зі світлого пластиліну виготовте вісім кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - три кульки, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок – моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедрі точки. Кульки - моделі атома Карбону - з'єднайте сірниками. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі пропану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. Підготуйте план складання моделі цієї молекули.<br>
| + | ЛАБОРАТОРНИЙ ДОСЛІД<br> |
| | | | |
| - | Інструкція 4. Змоделюйте молекулу бутану. Для цього зі світлого пластиліну виготовте десять кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - чотири кульки, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок -моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедра точки. Кульки - моделі атома Карбону - з'єднайте сірниками. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі бутану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. З'ясуйте, чи можливе обертання навколо зв'язків С-С. Підготуйте план складання моделі цієї молекули.<br>
| + | ''№ 6. Виготовлення моделей молекул вуглеводнів''<br> |
| | | | |
| - | Інструкція 5. Змоделюйте молекулу пентану. Для цього зі світлого пластиліну виготовте дванадцять кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - п'ять кульок, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок -моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедра точки. Кульки - моделі атома Карбону - з'єднайте сірниками. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників ви витратили для моделювання хімічних зв'язків між атомами? Яка валентність Карбону у молекулі пентану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. З'ясуйте, чи можливе обертання навколо зв'язків С-С. Підготуйте план складання моделі цієї молекули.<br>
| + | Завдання. Виготовте моделі молекул метану, етану, пропану, бутану, пентану та підготуйте план складання моделей.<br> |
| | | | |
| - | Інструкції для «домашніх» груп<br>
| + | Обладнання: пластилін темного і світлого кольорів, сірники або набір для складання кулестержневих моделей молекул.<br> |
| | | | |
| - | Порівняйте плани моделювання та моделі молекул метану, етану, пропану, бутану, пентану. У чому їх подібність і відмінність? Яка валентність Карбону в молекулах вуглеводнів? Чим зумовлена зигзагувата будова карбонового ланцюга? Чи можливе вільне обертання атомів навколо карбон-карбонових зв'язків? Поясніть, для чого моделюють молекули речовин.<br>
| + | Порада. Об'єднайтеся в «домашні» групи з п'ятьох учнів, ознайомтеся із завданням: кожен з вас має вибрати вуглеводень, який моделюватиме. Перейдіть до «робочої» групи - усі її члени виготовлятимуть модель одного й того самого вуглеводню. Ви зможете порівняти з роботами інших учнів власноруч виготовлену модель та разом скласти план її виготовлення. Потім поверніться до своєї «домашньої» групи, аби продемонструвати свій доробок і узагальнити здобуті знання та вміння. Порівняйте готові моделі і складені плани, виокремте ті пункти плану, які можна використати для самоконтролю.<br> |
| | | | |
| - | • ''Назви гомологів метану ''(табл. 22.1), безсумнівно, не залишилися поза за вашою увагою - адже всі вони мають однаковий суфікс (який?). Він вказує на приналежність вуглеводню до гомологічного ряду метану або, іншими словами, - алканів. Корені у назвах перших чотирьох гомологів цього ряду походять з грецької й пов'язані з назвами спиртів або органічних кислот. Ці спирти й кислоти (деякі з них ви вивчатимете згодом) були відомі задовго до відкриття відповідних алканів. Приміром, етиловий (винний) спирт був відомий значно раніше за етан, отриманий лише 1848 року. Починаючи з пентану, назви алканів походять від грецьких числівників, які показують кількість атомів Карбону в молекулі алкану.<br>
| + | Інструкції для «робочих» груп<br> |
| | | | |
| - | <u>''Завдання''</u><br>
| + | Інструкція 1. Змоделюйте молекулу метану. Для цього зі світлого пластиліну виготовте чотири кульки діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - одну кульку, діаметр якої в 1,5 раза більший за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену й Карбону. На поверхні моделі атома Карбону позначте чотири рівновіддалені по кутах тетраедра точки. Вставте в них сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі метану? Перевірте чи дорівнюють кути між зв'язками 109,5°. Підготуйте план складання моделі цієї молекули.<br> |
| | | | |
| - | За таблицею 22.1 визначте, що означають грецькі числівники penta- та hepta-.<br>
| + | Інструкція 2. Змоделюйте молекулу етану. Для цього зі світлого пластиліну виготовте шість кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - дві кульки, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок - моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедрі точки. Обидві кульки з'єднайте сірником. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі етану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. Підготуйте план складання моделі цієї молекули.<br> |
| | | | |
| - | Поняття гомології в органічній хімії ґрунтується на фундаментальному положенні про те, що хімічні й фізичні властивості речовини визначаються складом і структурою її молекул. Пересвідчитися в цьому на прикладі гомологів метану ви зможете під час вивчення наступного параграфа.<br>
| + | Інструкція 3. Змоделюйте молекулу пропану. Для цього зі світлого пластиліну виготовте вісім кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - три кульки, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок – моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедрі точки. Кульки - моделі атома Карбону - з'єднайте сірниками. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі пропану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. Підготуйте план складання моделі цієї молекули.<br> |
| | | | |
| - | <u>''Стисло про головне<br>''</u>
| + | Інструкція 4. Змоделюйте молекулу бутану. Для цього зі світлого пластиліну виготовте десять кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - чотири кульки, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок -моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедра точки. Кульки - моделі атома Карбону - з'єднайте сірниками. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі бутану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. З'ясуйте, чи можливе обертання навколо зв'язків С-С. Підготуйте план складання моделі цієї молекули.<br> |
| | | | |
| - | Гомологи метану (алкани) входять до складу багатьох широковідомих споживчих продуктів - парафіну, гасу, газового пального, вазеліну, бензину тощо.<br>Вуглеводні - органічні сполуки, які складаються з атомів двох елементів - Карбону і Гідрогену. Хімічний склад алканів - вуглеводнів гомологічного ряду метану - описує загальна формула С<sub>n</sub>H<sub>2n+2</sub>, де n - додатне ціле число.
| + | Інструкція 5. Змоделюйте молекулу пентану. Для цього зі світлого пластиліну виготовте дванадцять кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - п'ять кульок, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок -моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедра точки. Кульки - моделі атома Карбону - з'єднайте сірниками. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників ви витратили для моделювання хімічних зв'язків між атомами? Яка валентність Карбону у молекулі пентану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. З'ясуйте, чи можливе обертання навколо зв'язків С-С. Підготуйте план складання моделі цієї молекули.<br> |
| | | | |
| - | Гомологи - речовини з однаковим якісним складом, подібні за будовою і хімічними властивостями. За кількісним складом вони відрізняються один від одного на групу -СН<sub>2</sub>- - гомологічну різницю. Гомологи, розташовані за зростанням їхньої відносної молекулярної маси, утворюють гомологічний ряд.
| + | Інструкції для «домашніх» груп<br> |
| | | | |
| - | Гомологічні ряди можна побудувати для всіх класів органічних сполук. Знаючи властивості одного з членів гомологічного ряду, можна дійти висновків щодо властивостей інших представників того самого ряду. Це й зумовлює важливість поняття гомології під час вивчення органічної хімії.
| + | Порівняйте плани моделювання та моделі молекул метану, етану, пропану, бутану, пентану. У чому їх подібність і відмінність? Яка валентність Карбону в молекулах вуглеводнів? Чим зумовлена зигзагувата будова карбонового ланцюга? Чи можливе вільне обертання атомів навколо карбон-карбонових зв'язків? Поясніть, для чого моделюють молекули речовин.<br> |
| | | | |
| - | В алканах атоми Карбону сполучені між собою тільки простими (одинарними, або ординарними) зв'язками, а решта зв'язків з'єднує їх атомами Гідрогену:<br><br>Такі зв'язки також називають одинарними.
| + | • ''Назви гомологів метану ''(табл. 22.1), безсумнівно, не залишилися поза за вашою увагою - адже всі вони мають однаковий суфікс (який?). Він вказує на приналежність вуглеводню до гомологічного ряду метану або, іншими словами, - алканів. Корені у назвах перших чотирьох гомологів цього ряду походять з грецької й пов'язані з назвами спиртів або органічних кислот. Ці спирти й кислоти (деякі з них ви вивчатимете згодом) були відомі задовго до відкриття відповідних алканів. Приміром, етиловий (винний) спирт був відомий значно раніше за етан, отриманий лише 1848 року. Починаючи з пентану, назви алканів походять від грецьких числівників, які показують кількість атомів Карбону в молекулі алкану.<br> |
| | | | |
| - | У метані та його гомологах зв'язки між атомами розміщені в просторі під кутом 109,5°. Тому молекула найпростішого алкану має тетраедричну форму, у молекулі етану два атоми Карбону розташовані на одній прямій, а молекули решти алканів набувають зигзагуватої форми.
| + | <u>''Завдання''</u><br> |
| | | | |
| - | Починаючи з етану, виникає можливість обертання навколо ординарно зв'язку С-С. Внаслідок цього молекули алканів можуть набувати різноманітних геометричних форм. Молекулам алканів з понад двома атомами Карбону в ланцюзі властиві вигнуті форми.
| + | За таблицею 22.1 визначте, що означають грецькі числівники penta- та hepta-.<br> |
| | | | |
| - | Назви гомологів метану мають однаковий суфікс -ан. Він вказує на приналежність вуглеводню до гомологічного ряду метану або, іншими словами, - алканів. Корені в назвах перших чотирьох гомологів цього ряду походять з грецької і пов'язані з назвами спиртів або органічних квот. Починаючи з пентану, назви алканів походять від грецьких числівників.
| + | Поняття гомології в органічній хімії ґрунтується на фундаментальному положенні про те, що хімічні й фізичні властивості речовини визначаються складом і структурою її молекул. Пересвідчитися в цьому на прикладі гомологів метану ви зможете під час вивчення наступного параграфа.<br> |
| | | | |
| - | <u>''Застосуйте свої знання й уміння''</u> | + | <u>''Стисло про головне<br>''</u> |
| | | | |
| - | 1. Назвіть перші 5 членів гомологічного ряду метану з непарною кількістю атомів Карбону в молекулі.
| + | Гомологи метану (алкани) входять до складу багатьох широковідомих споживчих продуктів - парафіну, гасу, газового пального, вазеліну, бензину тощо.<br>Вуглеводні - органічні сполуки, які складаються з атомів двох елементів - Карбону і Гідрогену. Хімічний склад алканів - вуглеводнів гомологічного ряду метану - описує загальна формула С<sub>n</sub>H<sub>2n+2</sub>, де n - додатне ціле число. |
| | | | |
| - | 2. Виберіть загальну формулу вуглеводнів гомологічного ряду метану: <br>А С<sub>n</sub>Н<sub>2n</sub>; Б С<sub>n</sub>Н<sub>2n-2</sub>; В С<sub>n</sub>Н<sub>n+2</sub>; Г С<sub>n</sub>Н<sub>2n+2</sub>.
| + | Гомологи - речовини з однаковим якісним складом, подібні за будовою і хімічними властивостями. За кількісним складом вони відрізняються один від одного на групу -СН<sub>2</sub>- - гомологічну різницю. Гомологи, розташовані за зростанням їхньої відносної молекулярної маси, утворюють гомологічний ряд. |
| | | | |
| - | 3. Алкан з найдовшими молекулами синтезували 1985 р. англійські хіміки І. Бідд і М.К. Уайтинг. Це нонаконтатриктан, молекула якого містить 390 атомів Карбону, Виберіть кількість атомів Гідрогену у молекулі цієї речовини:<br>А 197; Б 390; В 780; Г 782.
| + | Гомологічні ряди можна побудувати для всіх класів органічних сполук. Знаючи властивості одного з членів гомологічного ряду, можна дійти висновків щодо властивостей інших представників того самого ряду. Це й зумовлює важливість поняття гомології під час вивчення органічної хімії. |
| | | | |
| - | 4. Визначте молекулярну формулу алкану, масова частка Карбону в якому становить 85 %.
| + | В алканах атоми Карбону сполучені між собою тільки простими (одинарними, або ординарними) зв'язками, а решта зв'язків з'єднує їх атомами Гідрогену: |
| | | | |
| - | 5. Складіть молекулярну, електронну та структурні (повну та спрощену) формули алкану: а) відносна молекулярна маса якого дорівнює 30; б) відносна густина за воднем якого дорівнює 22.
| + | [[Image:Chemistry_154.jpg]] |
| | | | |
| - | 6. Виберіть ознаку, притаманну членам одного гомологічного ряду:<br>А Однаковий якісний склад; Б Однаковий кількісний склад; В Однакова молекулярна маса; Г Однакова густина за повітрям.
| + | Такі зв'язки також називають одинарними. |
| | | | |
| - | 7. Виберіть число, на яке відрізняються відносні молекулярні маси двох сусідніх гомологів: А 12; Б 14; В 16; Г 18.
| + | У метані та його гомологах зв'язки між атомами розміщені в просторі під кутом 109,5°. Тому молекула найпростішого алкану має тетраедричну форму, у молекулі етану два атоми Карбону розташовані на одній прямій, а молекули решти алканів набувають зигзагуватої форми. |
| | | | |
| - | 8. Виберіть правильні твердження. У молекулах алканів усі хімічні зв'язки:<br>А Ковалентні; Б Ординарні; В Йонні; Г Подвійні; В Неполярні; Г Потрійні.
| + | Починаючи з етану, виникає можливість обертання навколо ординарно зв'язку С-С. Внаслідок цього молекули алканів можуть набувати різноманітних геометричних форм. Молекулам алканів з понад двома атомами Карбону в ланцюзі властиві вигнуті форми. |
| | | | |
| - | 9. Назвіть гомолог метану, починаючи з якого виникає можливість обертання навколо ординарного зв'язку С-С.
| + | Назви гомологів метану мають однаковий суфікс -ан. Він вказує на приналежність вуглеводню до гомологічного ряду метану або, іншими словами, - алканів. Корені в назвах перших чотирьох гомологів цього ряду походять з грецької і пов'язані з назвами спиртів або органічних квот. Починаючи з пентану, назви алканів походять від грецьких числівників. |
| | | | |
| - | 10. Виберіть суфікс, притаманний назвам гомологів метану: А -он; Б -eн; В -ан; Г -ин.
| + | <u>''Застосуйте свої знання й уміння''</u> |
| | | | |
| - | 11. Розташуйте алкани за зменшенням їхніх відносних молекулярних мас: А Нонан; Б Пропан; В Октан; Г Гексан.
| + | 1. Назвіть перші 5 членів гомологічного ряду метану з непарною кількістю атомів Карбону в молекулі. |
| | | | |
| - | 12. Розташуйте алкани за зростанням їхніх відносних густин за киснем: А Етан; Б Пропан; В Метан; Г Бутан. | + | 2. Виберіть загальну формулу вуглеводнів гомологічного ряду метану: <br>А С<sub>n</sub>Н<sub>2n</sub>; Б С<sub>n</sub>Н<sub>2n-2</sub>; В С<sub>n</sub>Н<sub>n+2</sub>; Г С<sub>n</sub>Н<sub>2n+2</sub>. |
| | + | |
| | + | 3. Алкан з найдовшими молекулами синтезували 1985 р. англійські хіміки І. Бідд і М.К. Уайтинг. Це нонаконтатриктан, молекула якого містить 390 атомів Карбону, Виберіть кількість атомів Гідрогену у молекулі цієї речовини:<br>А 197; Б 390; В 780; Г 782. |
| | + | |
| | + | 4. Визначте молекулярну формулу алкану, масова частка Карбону в якому становить 85 %. |
| | + | |
| | + | 5. Складіть молекулярну, електронну та структурні (повну та спрощену) формули алкану: а) відносна молекулярна маса якого дорівнює 30; б) відносна густина за воднем якого дорівнює 22. |
| | + | |
| | + | 6. Виберіть ознаку, притаманну членам одного гомологічного ряду:<br>А Однаковий якісний склад; Б Однаковий кількісний склад; В Однакова молекулярна маса; Г Однакова густина за повітрям. |
| | + | |
| | + | 7. Виберіть число, на яке відрізняються відносні молекулярні маси двох сусідніх гомологів: А 12; Б 14; В 16; Г 18. |
| | + | |
| | + | 8. Виберіть правильні твердження. У молекулах алканів усі хімічні зв'язки:<br>А Ковалентні; Б Ординарні; В Йонні; Г Подвійні; В Неполярні; Г Потрійні. |
| | + | |
| | + | 9. Назвіть гомолог метану, починаючи з якого виникає можливість обертання навколо ординарного зв'язку С-С. |
| | + | |
| | + | 10. Виберіть суфікс, притаманний назвам гомологів метану: А -он; Б -eн; В -ан; Г -ин. |
| | + | |
| | + | 11. Розташуйте алкани за зменшенням їхніх відносних молекулярних мас: А Нонан; Б Пропан; В Октан; Г Гексан. |
| | + | |
| | + | 12. Розташуйте алкани за зростанням їхніх відносних густин за киснем: А Етан; Б Пропан; В Метан; Г Бутан. |
| | | | |
| | 13. Виберіть формулу алкану, у якому масова частка Карбону втричі більша за масову частку Гідрогену:<br>А Метан; Б Етан; В Бутан; Г Пентан.<br><br><u>Моделі молекул. Значення моделювання в хімії. Структурні формули органічних речовин</u><br> | | 13. Виберіть формулу алкану, у якому масова частка Карбону втричі більша за масову частку Гідрогену:<br>А Метан; Б Етан; В Бутан; Г Пентан.<br><br><u>Моделі молекул. Значення моделювання в хімії. Структурні формули органічних речовин</u><br> |
Версия 15:10, 7 апреля 2010
Гіпермаркет Знань>>Хімія>>Хімія 9 клас>> Хімія: Гомологи метану, їх фізичні властивості. Молекулярні та структурні формули, назви. Моделі молекул. Значення моделювання в хімії
ГОМОЛОГИ МЕТАНУ. ФІЗИЧНІ ВЛАСТИВОСТІ ГОМОЛОГІВ МЕТАНУ. МОЛЕКУЛЯРНІ ТА СТРУКТУРНІ ФОРМУЛИ, НАЗВИ. МОДЕЛІ МОЛЕКУЛ. ЗНАЧЕННЯ МОДЕЛЮВАННЯ В ХІМІЇ
Гомологи метану. Молекулярні та структурні формули, назви.
Після опрацювання § 22 ви зможете:
називати перші 10 членів гомологічного ряду метану, загальну формулу цього ряду; складати молекулярні, електронні та структурні формули гомологів метану й пояснювати їх; збирати моделі молекул гомологів метану; пояснювати суть гомології.
На шляху до успіху пригадаємо з вивчених курсів хімії:
що таке кристалогідрати; як визначають карбон (IV) оксид; яку будову має молекула метану; як складають електронні формули речовин; що таке спрощена структурна формула і як її перетворити на повну структурну формулу речовини.
• Гомологи метану (алкани) трапляться у нашому житті чи не на кожному кроці (мал. 22.1). Вони - компоненти природного і попутного нафтового газу, нафти.

Що означає слово «гомолог»? У перекладі з давньогрецької 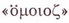 означає «подібний, схожий», а означає «подібний, схожий», а  - «слово», «закон». Чим саме подібні до метану та між собою його гомологи? - «слово», «закон». Чим саме подібні до метану та між собою його гомологи?
Елементний склад численних гомологів метану з'ясуймо за допомогою простого досліду (мал. 22.2). Продукти згоряння парафіну пропустімо послідовно через безводний купрум(ІІ) сульфат і водний розчин кальцій гідроксиду (вапняну воду).

Помутніння вапняної води зумовлює продукт повного окиснення парафіну карбон(IV) оксид. Його утворення під час горіння парафіну є підставою стверджувати, що у складі гомологів метану є Карбон. Кіптява, яка утворюється під час неповного згоряння парафіну, також свідчить про наявність Карбону у складі його компонентів.
Завдання
Запишіть рівняння реакції між карбон(IV) оксидом і кальцій гідроксидом. Класифікуйте цю хімічну реакцію.
Другий продукт повного окиснення парафіну - вода. Отже, до складу гомологів метану входить Гідроген.
Завдання
Опишіть зміну кольору безводного купрум(ІІ) сульфату (мал. 22.2). Запишіть хімічне рівняння, яке пояснює ці зміни (див. § 5).
Якісний і кількісний аналіз довели, що будь-який гомолог метану містить лише два хімічні елементи - Карбон і Гідроген. Такі речовини називають вуглеводнями. Однак не всі вуглеводні є гомологами метану. До них належать лише ті, склад яких описує загальна формула СnН2n+2, де n - додатне ціле число. Наприклад, молекулярна формула алкану, у складі якого 4 атоми Карбону, - С4Н10.
Завдання
Запишіть молекулярні формули алканів, у складі яких: а) 2; б) 5; в) 17 атомів Карбону.
Отже, поміж розмаїття органічних сполук можна виокремити речовини з однаковим якісним складом, подібні за будовою і хімічними властивостями. Такі речовини називають гомологами. За кількісним складом вони відрізняються один від одного на певну кількість груп -СН2-. Групу -СН2- називають гомологічною різницею. Гомологи, розташовані за зростанням їхньої відносної молекулярної маси, утворюють гомологічний ряд. Формула будь-якого наступного гомолога може бути отримана додаванням гомологічної різниці до формули попереднього члена гомологічного ряду.
Завдання
Поясніть, як, знаючи хімічну формулу гексану С6Н14, визначити формулу гомолога, який у гомологічному ряду: а) передує йому; б) розташований після нього.
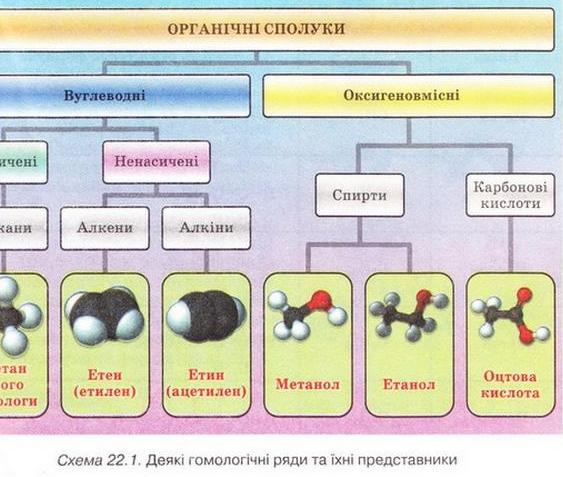
Зауважмо, що гомологічні ряди можна побудувати для всіх класів органічних сполук. Приміром, на схемі 22.1 зазначено назви деяких органічних речовин, з якими ви ознайомитеся цього року. Кожна зі сполук є представником певного гомологічного ряду. Проте не обов'язково докладно вивчати усі представники ряду. Адже знаючи властивості одне: і з членів гомологічного ряду, можна дійти висновків щодо властиве і інших представників того ж ряду. Це й зумовлює важливість поняття гомології під час вивчення органічної хімії.
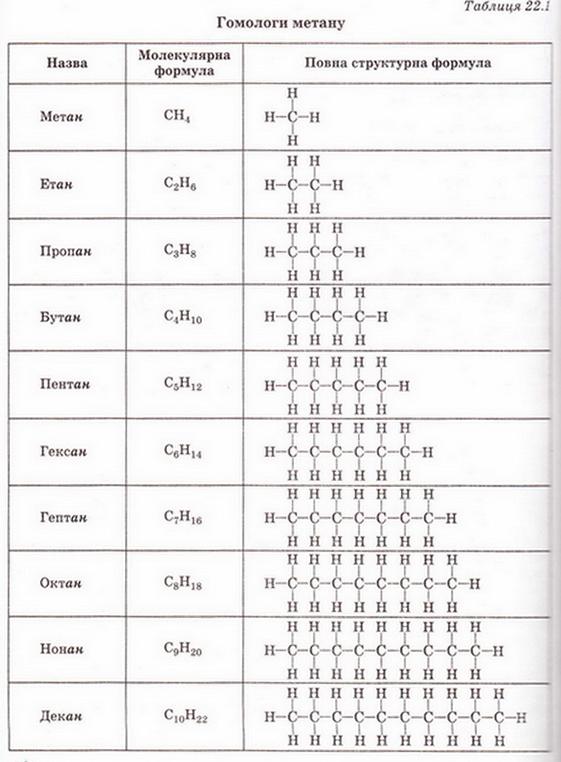
• Молекулярні та структурні формули, назви перших десяти членів гомологічного ряду метану представлені у таблиці 22.1. Зверніть увагу на наведені у ній повні структурні формули алканів: кожний наступні гомолог метану виведено з попереднього. Це може бути зроблено заміщенням на групу -СН3 одного з атомів Гідрогену або розташуванням групи -СН2- між двома сусідніми атомами Карбону (мал. 22.3).
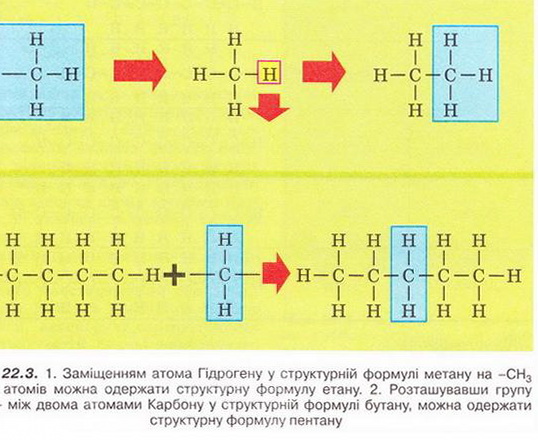
Завдання
Виведіть двома способами структурну формулу гептану зі структурної формули гексану.
Завдання
1. Запишіть електронні формули пропану та пентану. 2. Проаналізуйте зміст таблиці 22.1 і визначте, чи справедливі загальні закономірності зміни кількісного складу гомологів для представників гомологічного ряду метану.
Повні структурні формули відображують послідовність розміщення атомів Карбону і Гідрогену. З них очевидно, що в алканах атоми Карбону сполучені між собою тільки одинарними (простими, ординарними) зв'язками, а решта зв'язків з'єднує їх з атомами Гідрогену. Аби з'ясувати, як атоми Карбону і Гідрогену розміщені один відносно одного у просторі, звернімося до матеріальних моделей алканів (мал. 22.4).
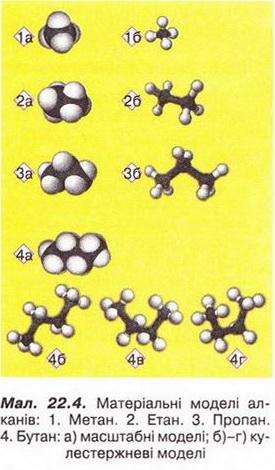
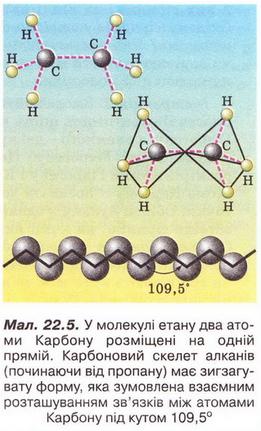
У метані та його гомологах зв'язки між атомами розміщені в просторі під кутом 109,5°. Тому молекула найпростішого алкану має тетраедричну форму, у молекулі етану два атоми Карбону розташовані на одній прямій, а молекули решти алканів набувають зигзагуватої форми (мал. 22.5).
Завдання
За спрощеними структурними формулами деяких алканів запишіть їхні повні структурні й електронні формули:
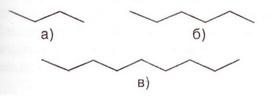
Починаючи від етану виникає живість обертання навколо ординарного зв'язку С - С. Внаслідок цього молекули алканів можуть набувати різноманітних геометричних форм (мал. 22.4, 4, а - г). Молекулам алканів з понад двома атомами Карбону в ланцюзі властиві вигнуті форми.
Найміцніше засвоюється інформація, одержувана під час самостійного спостереження або дослідження. Аби на власні очі (радше сказати, власноруч) пересвідчитися у зигзагуватій будові карбонового ланцюга і можливостях обертання атомів навколо карбон-карбонових зв’язків, виконайте лабораторний дослід.
ЛАБОРАТОРНИЙ ДОСЛІД
№ 6. Виготовлення моделей молекул вуглеводнів
Завдання. Виготовте моделі молекул метану, етану, пропану, бутану, пентану та підготуйте план складання моделей.
Обладнання: пластилін темного і світлого кольорів, сірники або набір для складання кулестержневих моделей молекул.
Порада. Об'єднайтеся в «домашні» групи з п'ятьох учнів, ознайомтеся із завданням: кожен з вас має вибрати вуглеводень, який моделюватиме. Перейдіть до «робочої» групи - усі її члени виготовлятимуть модель одного й того самого вуглеводню. Ви зможете порівняти з роботами інших учнів власноруч виготовлену модель та разом скласти план її виготовлення. Потім поверніться до своєї «домашньої» групи, аби продемонструвати свій доробок і узагальнити здобуті знання та вміння. Порівняйте готові моделі і складені плани, виокремте ті пункти плану, які можна використати для самоконтролю.
Інструкції для «робочих» груп
Інструкція 1. Змоделюйте молекулу метану. Для цього зі світлого пластиліну виготовте чотири кульки діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - одну кульку, діаметр якої в 1,5 раза більший за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену й Карбону. На поверхні моделі атома Карбону позначте чотири рівновіддалені по кутах тетраедра точки. Вставте в них сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі метану? Перевірте чи дорівнюють кути між зв'язками 109,5°. Підготуйте план складання моделі цієї молекули.
Інструкція 2. Змоделюйте молекулу етану. Для цього зі світлого пластиліну виготовте шість кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - дві кульки, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок - моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедрі точки. Обидві кульки з'єднайте сірником. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі етану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. Підготуйте план складання моделі цієї молекули.
Інструкція 3. Змоделюйте молекулу пропану. Для цього зі світлого пластиліну виготовте вісім кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - три кульки, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок – моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедрі точки. Кульки - моделі атома Карбону - з'єднайте сірниками. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі пропану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. Підготуйте план складання моделі цієї молекули.
Інструкція 4. Змоделюйте молекулу бутану. Для цього зі світлого пластиліну виготовте десять кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - чотири кульки, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок -моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедра точки. Кульки - моделі атома Карбону - з'єднайте сірниками. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників потрібно для моделювання хімічних зв'язків між атомами? Яка валентність Карбону в молекулі бутану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. З'ясуйте, чи можливе обертання навколо зв'язків С-С. Підготуйте план складання моделі цієї молекули.
Інструкція 5. Змоделюйте молекулу пентану. Для цього зі світлого пластиліну виготовте дванадцять кульок діаметром 2,4 мм - моделі атомів Гідрогену, а з темного - п'ять кульок, діаметри яких у 1,5 раза більші за модель атома Гідрогену. Це приблизно передасть співвідношення розмірів атомів Гідрогену і Карбону. На поверхнях кульок -моделей атома Карбону - позначте чотири рівновіддалені по кутах тетраедра точки. Кульки - моделі атома Карбону - з'єднайте сірниками. У решту позначених точок вставте сірники, на кінці яких приєднайте моделі атомів Гідрогену. Скільки сірників ви витратили для моделювання хімічних зв'язків між атомами? Яка валентність Карбону у молекулі пентану? Перевірте, чи дорівнюють кути між зв'язками 109,5°. З'ясуйте, чи можливе обертання навколо зв'язків С-С. Підготуйте план складання моделі цієї молекули.
Інструкції для «домашніх» груп
Порівняйте плани моделювання та моделі молекул метану, етану, пропану, бутану, пентану. У чому їх подібність і відмінність? Яка валентність Карбону в молекулах вуглеводнів? Чим зумовлена зигзагувата будова карбонового ланцюга? Чи можливе вільне обертання атомів навколо карбон-карбонових зв'язків? Поясніть, для чого моделюють молекули речовин.
• Назви гомологів метану (табл. 22.1), безсумнівно, не залишилися поза за вашою увагою - адже всі вони мають однаковий суфікс (який?). Він вказує на приналежність вуглеводню до гомологічного ряду метану або, іншими словами, - алканів. Корені у назвах перших чотирьох гомологів цього ряду походять з грецької й пов'язані з назвами спиртів або органічних кислот. Ці спирти й кислоти (деякі з них ви вивчатимете згодом) були відомі задовго до відкриття відповідних алканів. Приміром, етиловий (винний) спирт був відомий значно раніше за етан, отриманий лише 1848 року. Починаючи з пентану, назви алканів походять від грецьких числівників, які показують кількість атомів Карбону в молекулі алкану.
Завдання
За таблицею 22.1 визначте, що означають грецькі числівники penta- та hepta-.
Поняття гомології в органічній хімії ґрунтується на фундаментальному положенні про те, що хімічні й фізичні властивості речовини визначаються складом і структурою її молекул. Пересвідчитися в цьому на прикладі гомологів метану ви зможете під час вивчення наступного параграфа.
Стисло про головне
Гомологи метану (алкани) входять до складу багатьох широковідомих споживчих продуктів - парафіну, гасу, газового пального, вазеліну, бензину тощо.
Вуглеводні - органічні сполуки, які складаються з атомів двох елементів - Карбону і Гідрогену. Хімічний склад алканів - вуглеводнів гомологічного ряду метану - описує загальна формула СnH2n+2, де n - додатне ціле число.
Гомологи - речовини з однаковим якісним складом, подібні за будовою і хімічними властивостями. За кількісним складом вони відрізняються один від одного на групу -СН2- - гомологічну різницю. Гомологи, розташовані за зростанням їхньої відносної молекулярної маси, утворюють гомологічний ряд.
Гомологічні ряди можна побудувати для всіх класів органічних сполук. Знаючи властивості одного з членів гомологічного ряду, можна дійти висновків щодо властивостей інших представників того самого ряду. Це й зумовлює важливість поняття гомології під час вивчення органічної хімії.
В алканах атоми Карбону сполучені між собою тільки простими (одинарними, або ординарними) зв'язками, а решта зв'язків з'єднує їх атомами Гідрогену:
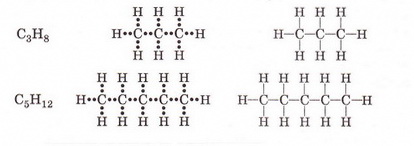
Такі зв'язки також називають одинарними.
У метані та його гомологах зв'язки між атомами розміщені в просторі під кутом 109,5°. Тому молекула найпростішого алкану має тетраедричну форму, у молекулі етану два атоми Карбону розташовані на одній прямій, а молекули решти алканів набувають зигзагуватої форми.
Починаючи з етану, виникає можливість обертання навколо ординарно зв'язку С-С. Внаслідок цього молекули алканів можуть набувати різноманітних геометричних форм. Молекулам алканів з понад двома атомами Карбону в ланцюзі властиві вигнуті форми.
Назви гомологів метану мають однаковий суфікс -ан. Він вказує на приналежність вуглеводню до гомологічного ряду метану або, іншими словами, - алканів. Корені в назвах перших чотирьох гомологів цього ряду походять з грецької і пов'язані з назвами спиртів або органічних квот. Починаючи з пентану, назви алканів походять від грецьких числівників.
Застосуйте свої знання й уміння
1. Назвіть перші 5 членів гомологічного ряду метану з непарною кількістю атомів Карбону в молекулі.
2. Виберіть загальну формулу вуглеводнів гомологічного ряду метану:
А СnН2n; Б СnН2n-2; В СnНn+2; Г СnН2n+2.
3. Алкан з найдовшими молекулами синтезували 1985 р. англійські хіміки І. Бідд і М.К. Уайтинг. Це нонаконтатриктан, молекула якого містить 390 атомів Карбону, Виберіть кількість атомів Гідрогену у молекулі цієї речовини:
А 197; Б 390; В 780; Г 782.
4. Визначте молекулярну формулу алкану, масова частка Карбону в якому становить 85 %.
5. Складіть молекулярну, електронну та структурні (повну та спрощену) формули алкану: а) відносна молекулярна маса якого дорівнює 30; б) відносна густина за воднем якого дорівнює 22.
6. Виберіть ознаку, притаманну членам одного гомологічного ряду:
А Однаковий якісний склад; Б Однаковий кількісний склад; В Однакова молекулярна маса; Г Однакова густина за повітрям.
7. Виберіть число, на яке відрізняються відносні молекулярні маси двох сусідніх гомологів: А 12; Б 14; В 16; Г 18.
8. Виберіть правильні твердження. У молекулах алканів усі хімічні зв'язки:
А Ковалентні; Б Ординарні; В Йонні; Г Подвійні; В Неполярні; Г Потрійні.
9. Назвіть гомолог метану, починаючи з якого виникає можливість обертання навколо ординарного зв'язку С-С.
10. Виберіть суфікс, притаманний назвам гомологів метану: А -он; Б -eн; В -ан; Г -ин.
11. Розташуйте алкани за зменшенням їхніх відносних молекулярних мас: А Нонан; Б Пропан; В Октан; Г Гексан.
12. Розташуйте алкани за зростанням їхніх відносних густин за киснем: А Етан; Б Пропан; В Метан; Г Бутан.
13. Виберіть формулу алкану, у якому масова частка Карбону втричі більша за масову частку Гідрогену:
А Метан; Б Етан; В Бутан; Г Пентан.
Моделі молекул. Значення моделювання в хімії. Структурні формули органічних речовин
Після опрацювання § 19 ви зможете:
характеризувати моделювання як метод хімічної науки.
На шляху до успіху пригадаємо з вивчених курсів природничих наук які способи пізнання природи використовують у хімії; що означає префікс нано-; що таке модель і масштаб; як записують хімічні та електронні формули речовин.
• Моделі молекул, так само, як і моделі атомів або кристалів, допомагають зримо уявити реальні об'єкти, безпосереднє спостереження за якими проводити незручно або неможливо.
Завдання
Встановіть відповідність між науками і моделями, які вони зазвичай використовують.
|
Наука
1 Географія
2 Фізика
3 Біологія
4 Хімія
|
Модель
А Електрофорна машина
Б Глобус
В Схема будови деревообробного верстата
Г Схема виробництва амоніаку
Д Муляж серця
|
Моделювання - це вивчення явища або об'єкта за допомогою його замінників, аналогів (моделей).
• Значення моделювання в хімії важко переоцінити. За його допомогою науковці пояснюють закони природи, перевіряють гіпотези, прогнозують існування об'єктів та явищ, які дотепер не спостерігли.
Приміром, модель трубчастого вуглецю описав на сторінках часопис «Хімія і життя» відомий український хімік-органік Михайло Корнілов ще 1985 р. А вже у 1991 р. науковці синтезували перші нанотрубки з атомів цього елемента.
Умовно хімічні моделі поділяють на знакові (символьні) та матеріальні. Знакові моделі - це символи елементів, хімічні формули, рівняння реакцій тощо. Матеріальні моделі - моделі атомів, йонів, кристалів, молекул, хімічних приладів і промислових апаратів хімічних виробництв.
Завдання
Пригадайте, як відбуваються реакції електролітами у розчині. Оцініть відповідність моделей (мал. 19.1) реальному процесу нейтралізації кислоти лугом у розчині. Зобразіть знакову модель, яка більш реалістично відображає суть реакції нейтралізації.

Розмаїтий барвистий світ молекул і кристалів та процесів за їхньою участю найліпше спостерігати на екрані комп'ютера. Сучасні графічні програми дають змогу поринути у віртуальну реальність мікро- та макросвіту, вивчати об'єкти в статиці та русі, керувати ними (мал. 19.2).
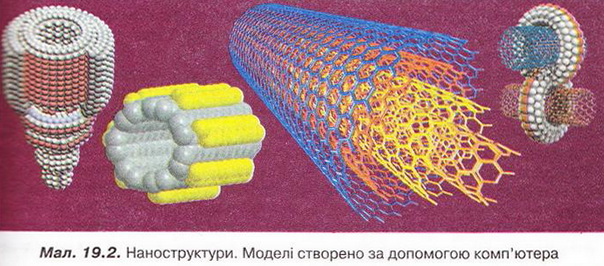
Для моделювання молекул найчастіше використовують кулестержневі та об'ємні (масштабні) моделі. Зверніть увагу: моделі лише відображають структуру мікрооб'єктів, принципи їхньої будови, однак не відтворюють зовнішнього вигляду.
У кулестержневих моделях кулі зображують ядра атомів, а стержні - напрямки хімічних зв'язків та величини кутів між ними. Розмір атомного ядра становить близько 10-15 м (для легких ядер), а розмір самого атома близько 10-10 м. Тобто, якщо використати для моделі ядра кульку діаметром 1 см, розмір моделі самого атома становитиме близько кілометра. Тому реальними співвідношеннями розмірів у цих моделях доводиться поступатися. Натомість об'ємні (масштабні) моделі відображають реальні співвідношення між розмірами атомів.
Завдання
Пригадайте, що таке масштаб. Поясніть, чи є підстави об'ємні моделі називані масштабними.
Традиційно моделі атомів Карбону та їхніх ядер мають чорне забарвлення, Гідрогену - біле, Нітрогену - синє, Оксигену - червоне, Сульфуру жовте, Хлору - зелене.
Через складність будови молекул багатьох органічних сполук кулестержневі й особливо об'ємні моделі втрачають наочність, оскільки справляють враження купи безладно розміщених різнокольорових кульок. З огляду на це склад і будову молекул органічних речовин доцільніше моделювати дещо спрощено, за допомогою знакових моделей(мал. 19.3).
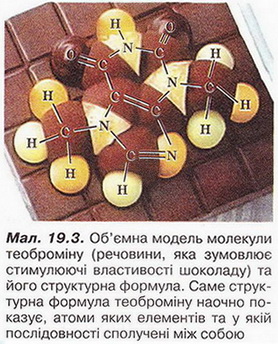
Стисло про головне
Моделі молекул, так само, як і моделі атомів, кристалів тощо, допомагають зримо уявити собі реальні об'єкти, безпосереднє спостереження за ЯКИМИ проводити незручно або неможливо.
Моделювання - це вивчення явища або об'єкта за допомогою його замінників, аналогів (моделей). За його допомогою науковці пояснюють закони природи, перевіряють гіпотези, прогнозують існування об'єктів та явищ, які дотепер не спостерігали.
Хімічні моделі умовно поділяють на знакові (символьні) та матеріальні, - Знакові моделі - це символи елементів, хімічні формули, рівняння реакцій тощо. Матеріальні моделі - моделі атомів, йонів, кристалів, молекул, хімічних приладів і промислових апаратів хімічних виробництв.
Для моделювання молекул найчастіше використовують кулестержневі та об'ємні моделі. Вони лише відображають структуру мікрооб'єктів, принципи їхньої будови, однак не відтворюють зовнішнього вигляду.
У кулестержневих моделях кулі зображують ядра атомів, а стержні - напрямки хімічних зв'язків та величини кутів між ними. Об'ємні моделі відбивають реальні співвідношення між розмірами атомів.
Застосуйте свої знання й уміння
1. Назвіть моделі, які вам доводилося використовувати під час вивчення природничих і точних наук.
2. Поясніть, для чого застосовують моделювання в хімії.
3. Наведіть приклади матеріальних і знакових моделей, які використовують у хімії.
4. Порівняйте кулестержневі та об'ємні моделі молекул.
Скарбничка досвіду
З наступного параграфа ви дізнаєтеся, який науковець запровадив кулестержневі моделі органічних сполук. А хто започаткував використанню масштабних моделей? З'ясуйте це, використовуючи різноманітні джерела інформації. За результатами дослідження підготуйте презентацію.
Г. А. Лашевська, Геометрія, 9 клас
Вислано читачами з інтернет-сайтів
Скачати календарно-тематичне планування з хімії, відповіді на тести, завдання та відповіді школяру, книги та підручники, курси учителю з хімії для 9 класу
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|






















